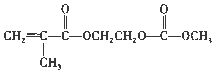题目内容
【题目】![]() ,101kPa时,强酸与强碱的稀溶液发生中和反应生成1mol水时所放出的热量约为
,101kPa时,强酸与强碱的稀溶液发生中和反应生成1mol水时所放出的热量约为![]() ;辛烷的燃烧热为
;辛烷的燃烧热为![]() 下列热化学方程式书写正确的是( )
下列热化学方程式书写正确的是( )
A.![]()
B.![]()
C.![]()
![]()
![]()
![]()
D.![]()
![]()
![]()
【答案】D
【解析】
A. 中和热是强酸与强碱的稀溶液发生中和反应生成1mol水时放出的热量,醋酸是弱酸,电离要吸热;
B. 中和热是强酸与强碱的稀溶液发生中和反应生成1mol水时放出的热量;
C. 燃烧热是1mol可燃物完全反应生成稳定氧化物时放出的热量;
D. 燃烧热是1mol可燃物完全反应生成稳定氧化物时放出的热量,反应热与化学计量数成正比。
A. 因醋酸是弱酸,电离要吸热,所以该反应的反应热H不是-57.3kJ/mol,故A错误;
B. 中和反应是放热反应,焓变为负值,该热化学方程式不符合中和热的概念,故B错误;
C. 燃烧热中,水是液态,该反应热化学方程式中生成的水是气体,故C错误;
D. 该热化学方程式中是2mol物质燃烧,所以反应热的数值是燃烧热的2倍,热化学方程式为:![]() ,故D正确;
,故D正确;
答案选D。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液。
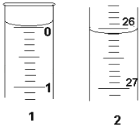
(1)若滴定开始和结束时,酸式滴定管中的液面如图所示:则所用盐酸的体积为__mL。滴定终点时的现象是:当滴入最后一滴盐酸时,锥形瓶中溶液颜色由___,且30s不恢复原色。
(2)某学生根据三次实验分别记录有关数据如下表:
滴定次数 | 待测氢氧化钠 溶液的体积/mL | 0.1000mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理数据算出该氢氧化钠溶液物质的量浓度(计算结果保留4位有效数字):c(NaOH)=__mol·L-1。
(3)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是__(填字母)。
A.滴定前滴定管中有气泡,滴定后消失 B.碱式滴定管量取NaOH溶液时,未进行润洗操作
C.滴定时达到滴定终点时俯视读数 D.锥形瓶取用NaOH待测液前加少量水洗涤