题目内容
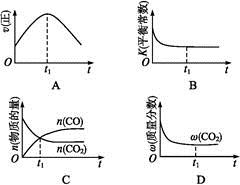
右图是可逆反应X2 + 3Y2 2Z2在反应过程中的反应速率(υ)与时间(t)的关系曲线,
2Z2在反应过程中的反应速率(υ)与时间(t)的关系曲线,
下列叙述正确的是

 2Z2在反应过程中的反应速率(υ)与时间(t)的关系曲线,
2Z2在反应过程中的反应速率(υ)与时间(t)的关系曲线,下列叙述正确的是

| A.t1时,只有正方向反应 | B.t2时,反应到达限度 |
| C.t2~ t3,反应不再发生 | D.t2~t3,各物质的浓度一定相等 |
B
试题分析:由图像可以看出该反应是可逆反应。反应是从正反应方向开始的,A.在达到平衡前,由于正反应速率大于逆反应速率,所以反应正向进行。由于在t1时还未达到平衡,所以反应正向进行。错误。B.在t2时达到了该反应条件下的平衡状态。正确。C.在t2~ t3,反应处于平衡状态,正反应与逆反应仍然在进行,只不过是单位时间内的任何物质的浓度都不发生变化,速率也都不发生不变。错误。D.t2~t3,反应处于平衡状态,各物质的浓度不变,但是它们的浓度不一定相等。错误。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。
bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。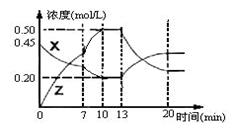
 CH3OH(g),根据题意,以下说法正确的是
CH3OH(g),根据题意,以下说法正确的是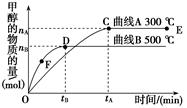
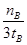 mol/(L·min)-1表示500 ℃以上反应在D点的速率
mol/(L·min)-1表示500 ℃以上反应在D点的速率 2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大
2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大 TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0
TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0
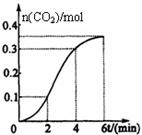
 CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.
CH3OH(g)+H2O(g)+49kJ。某科学实验将6molCO2和8molH2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标.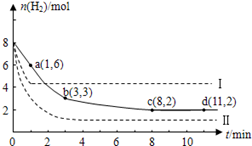
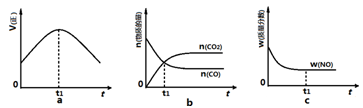
 2CO2(g)+ N2(g)。在密闭容器
2CO2(g)+ N2(g)。在密闭容器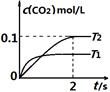
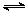 N2O4(g) △H=-56.9 kJ/mol ②
N2O4(g) △H=-56.9 kJ/mol ②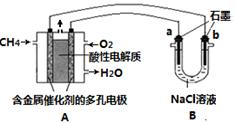
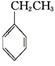 (g)+CO2(g)
(g)+CO2(g)
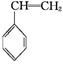 (g)+CO(g)+H2O(g)ΔH="-166" kJ·mol-1
(g)+CO(g)+H2O(g)ΔH="-166" kJ·mol-1