题目内容
9.现代原子结构理论认为,在同一电子层上,可有s、p、d、f、g、h…等亚层,各亚层分别有1、3、5、…个轨道.试根据电子填入轨道的顺序预测:(1)第8周期共有50 种元素;
(2)原子核外出现第一个6f电子的元素的原子序数是139;
(3)根据“稳定岛”假说,第114号元素是一种稳定同位素,半衰期很长,可能在自然界都可以找到.试推测第114号元素属于七 周期,IVA 族元素,原子的外围电子构型是7s27p2.
分析 (1)根据周期表中个周期元素的种数:2、8、8、18、18、32、32、50、50的递变规律来回答;
(2)原子核外出现第一个6f电子的元素的原子外围电子排布是6f77s2;
(3)根据零族元素的原子序数结合元素周期表的结构来确定元素的位置.
解答 解:(1)周期表中个周期元素的种数:2、8、8、18、18、32、32、50、50的递变规律排列的,所以第8周期共有50种元素,
故答案为:50;
(2)原子核外出现第一个6f电子的元素的原子外围电子排布是6f77s2,根据核外电子排布式,应该是:[118]5g186f18s2,属于139号元素,
故答案为:139;
(3)根据零族元素第七周期最后一个的原子序数是118,所以114号元素在此元素的左边,应该是第七周期,ⅣA族元素,属于p区元素,价电子排布是:7S27p2,
故答案为:七;ⅣA;7S27p2.
点评 本题考查了电子排布规律、元素周期表,是对物质结构化学知识的考查,侧重对基础知识的综合应用的考查,较好的考查学生分析推理能力,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列关于珠宝的描述错误的是( )
| A. | 珍珠上的污渍可以用酒精擦除,并用软布擦干后用脱脂棉包好保存 | |
| B. | 珊瑚、玛瑙和珍珠一样都可以作为重要药材 | |
| C. | 红宝石可以用于激光器,还可用于制作红宝石轴承 | |
| D. | 蓝宝石中含有变价元素铁、钛等 |
20.甲、乙两同学研究Na2SO3溶液与FeCl3溶液反应的情况.
(1)常温下,FeCl3溶液的pH<7(填“<”、“>”或“=”).
(2)分析红褐色产生的原因.
①甲同学认为步骤I中溶液呈红褐色是因为生成了Fe(OH)3,用化学平衡移动原理解释溶液呈红褐色的原因:Fe3++3H2O═Fe(OH)3+3H+,加入Na2SO3后,c(H+)下降,平衡正向移动,生成Fe(OH)3.
②乙同学认为可能是发生了氧化还原反应,完成并配平其反应的离子方程式:
□Fe3++□SO32-+□H2O═□F e2++□SO42-+□2H+
乙同学查阅资料得知:
(3)甲同学为了确认溶液呈红褐色的原因是生成了Fe(OH)3,设计并完成了如下实验:
甲同学因此得出结论:溶液呈红褐色是因为生成了Fe(OH)3.而乙同学认为甲同学得出结论的证据仍然不足,乙同学的理由是FeSO3和FeCl3的混合溶液也可能出现“丁达尔效应”.
(4)为进一步确认Na2SO3溶液与FeCl3溶液反应的情况,乙同学设计并完成了如下实验:
①经检验步骤III中红褐色溶液含有Fe2+,检验Fe2+选用的试剂是a(填字母).
a.K3[Fe(CN)6]溶液 b.KSCN溶液 c.KMnO4溶液
②已知H2SO3是弱酸,请结合电离方程式说明步骤III中出现红褐色的原因:H2SO3?H++HSO3-、HSO3-?H++SO32-,SO32-与被还原生成的Fe2+结合为FeSO3,与剩余的FeCl3溶液混合而呈现红褐色.
(5)结论:由上述实验得知,甲、乙两同学所持观点均正确.
| 步骤 | 操作 | 现象 |
| I | 向2mL 1mol•L-1FeCl3溶液中加入一定量的Na2SO3溶液 | 溶液由棕黄色变为红褐色, 并有少量刺激性气味的气体逸出 |
(2)分析红褐色产生的原因.
①甲同学认为步骤I中溶液呈红褐色是因为生成了Fe(OH)3,用化学平衡移动原理解释溶液呈红褐色的原因:Fe3++3H2O═Fe(OH)3+3H+,加入Na2SO3后,c(H+)下降,平衡正向移动,生成Fe(OH)3.
②乙同学认为可能是发生了氧化还原反应,完成并配平其反应的离子方程式:
□Fe3++□SO32-+□H2O═□F e2++□SO42-+□2H+
乙同学查阅资料得知:
| 1Fe2+与SO32-反应生成墨绿色的絮状沉淀FeSO3; 2墨绿色的FeSO3与黄色的FeCl3溶液混合后,溶液呈红褐色. |
| 步骤 | 操作 | 现象 |
| II | 用激光笔照射步骤I中的红褐色溶液 | 出现“丁达尔效应” |
(4)为进一步确认Na2SO3溶液与FeCl3溶液反应的情况,乙同学设计并完成了如下实验:
| 步骤 | 操作 | 现象 |
| III | 向1mol•L-1的FeCl3溶液中通入一定量的SO2 | 溶液由黄色变为红褐色 |
| IV | 用激光笔照射步骤III中的红褐色溶液 | 没有出现“丁达尔效应” |
a.K3[Fe(CN)6]溶液 b.KSCN溶液 c.KMnO4溶液
②已知H2SO3是弱酸,请结合电离方程式说明步骤III中出现红褐色的原因:H2SO3?H++HSO3-、HSO3-?H++SO32-,SO32-与被还原生成的Fe2+结合为FeSO3,与剩余的FeCl3溶液混合而呈现红褐色.
(5)结论:由上述实验得知,甲、乙两同学所持观点均正确.
17.下列分子或离子与SO42-互为等电子体的是( )
| A. | PCl5 | B. | CCl4 | C. | NF3 | D. | NH4+ |
4.下列说法正确的是( )
| A. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阴极的阳极保护法 | |
| B. | 石油的分馏、煤的液化、汽化都是物理变化 | |
| C. | 干馏煤可以得到甲烷、苯和氨等重要化工原料 | |
| D. | 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可以发生水解反应 |
18.有关如图所示化合物的说法不正确的是( )
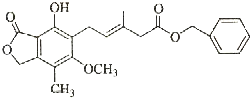

| A. | 既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应 | |
| B. | 既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 | |
| C. | 可以催化加氢,1mol该物质最多可与7mol H2反应 | |
| D. | 该化合物有4种官能团,可以使酸性KMnO4溶液褪色 |
19.下列事实中,可以证明NaCl中一定存在离子键的是( )
| A. | 有较高的熔点 | B. | 熔化时能导电 | C. | 水溶液能导电 | D. | 易溶于水 |