题目内容
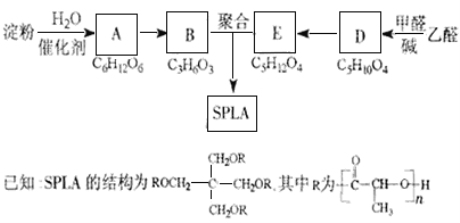
【题目】亚氯酸钠(NaC1O2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程,下列说法错误的是( )
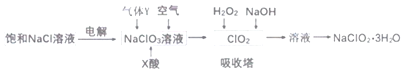
A.本工艺电解饱和氯化钠溶液时,阳极主要产生氯气,阴极产生氢气
B.吸收塔内的温度不宜过高
C.气体Y具有还原性
D.吸收塔中发生的离子反应为:H2O2+2OH-+2C1O2=2C1O2-+O2+2H2O
【答案】A
【解析】
根据流程可知,电解饱和氯化钠溶液,生成的氯气和氢氧化钠反应生成氯酸钠溶液,通气体Y、空气和X酸还原氯酸钠溶液生成二氧化氯,则气体Y具有还原性,再用双氧水、氢氧化钠吸收反应生成亚氯酸钠,过滤的亚氯酸钠(NaClO2)溶液通过蒸发浓缩冷却结晶得到亚氯酸钠晶体。
A.根据流程可知,电解饱和氯化钠溶液,阳极氯离子先失电子发生氧化反应产生氯气,氯气和阴极生成的氢氧化钠继续反应生成氯酸钠溶液,阴极氢离子得电子发生还原反应产生氢气,故A错误;
B.吸收塔内用双氧水、氢氧化钠吸收反应生成亚氯酸钠,因为温度过高,双氧水会分解,则吸收塔内的温度不宜过高,故B正确;
C.通气体Y、空气和X酸还原氯酸钠溶液生成二氧化氯,则气体Y具有还原性,故C正确;
D.吸收塔内用双氧水、氢氧化钠吸收反应生成亚氯酸钠,离子反应为:H2O2+2OH-+2C1O2=2C1O2-+O2+2H2O,故D正确;
综上所述,答案为A。

 寒假学与练系列答案
寒假学与练系列答案【题目】合成氨工业中的原料气制取与净化是重要的环节。
(1)已知有关反应的能量变化如图1:写出![]() 与
与![]() 反应制取
反应制取![]() 和
和![]() 的热化学方程式:______。
的热化学方程式:______。
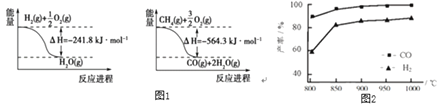
(2)“![]() 催化重整法”制氢气:
催化重整法”制氢气:![]() ,
,![]() 不仅可以得到合成气
不仅可以得到合成气![]() 和
和![]() ,还对温室气体的减排具有重要意义。上述反应中相关的化学键键能数据如表所示。
,还对温室气体的减排具有重要意义。上述反应中相关的化学键键能数据如表所示。
①根据键能计算,该反应的![]() ______
______![]() 。
。
化学键 | C-H | C=O | H-H |
|
键能kJ/mol | 413 | 745 | 436 | 1075 |
②按一定体积比加入![]() 和
和![]() ,在恒压下发生反应,温度对CO和
,在恒压下发生反应,温度对CO和![]() 产率的影响如图2所示。实际生产中此反应优选温度为900℃,原因是______。
产率的影响如图2所示。实际生产中此反应优选温度为900℃,原因是______。
③某温度下,将![]() 、
、![]() 以及催化剂进行加入
以及催化剂进行加入![]() 容器中,达到平衡时
容器中,达到平衡时![]() ,平衡常数
,平衡常数![]() ______
______![]() 。
。
(3)合成气在进入合成塔前常用醋酸二氨合铜![]() Ⅰ
Ⅰ![]() 溶液来吸收其中的CO杂质,其反应是:
溶液来吸收其中的CO杂质,其反应是:![]() ,必须除去原料气中CO的原因是______。醋酸二氨合铜
,必须除去原料气中CO的原因是______。醋酸二氨合铜![]() Ⅰ
Ⅰ![]() 吸收CO的生产适宜条件应是______
吸收CO的生产适宜条件应是______![]() 填序号
填序号![]() 。
。
A.高温高压 B.高温低压 C.低温高压 D.低温低压