题目内容
有关下列装置或操作说法错误的是( )
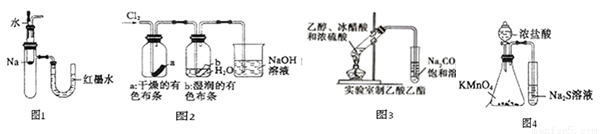
A.图1中:将胶头滴管中的水滴入到金属钠中,能看到U型管右侧红墨水上升
B.图2中:观察到湿润的有色布条能退色,待尾气全部被碱吸收后,将稀硫酸滴入烧杯中,至溶液显酸性,可能看到有黄绿色气体生成。
C.图3可用于制备乙酸乙酯
D.图4可以比较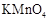 、
、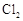 和S氧化性的相对强弱
和S氧化性的相对强弱
【答案】
C
【解析】
试题分析:图1中金属钠会与滴入的水发生反应放出大量的热,使得大试管中的气体膨胀压强增大,然后U形管的红墨水左边气压大于右边,所以右侧墨水升高,A正确;通过图2装置的气体使湿润的有色布条褪色,可以推测该气体为氯气,所以氯气被碱吸收后,生成Cl- 、ClO- ,如果在加入稀硫酸,发生反应2H++ Cl- +ClO- =Cl2+H2O,所以可观察到黄绿色气体生成,B正确;图3装置图收集乙酸乙酯的时候,导管不能插入到溶液中,否则会倒吸,所以C错误;图4加入浓盐酸到高锰酸钾中,可以制得Cl2,生成的Cl2通入到硫化钠溶液中可以制得黄色的硫沉淀,所以根据氧化还原反应,氧化剂还原性强于氧化产物的规律,可比较得出氧化性KMnO4> Cl2>S,D正确,故选C.
考点:本题考查的是基础实验装置和设计。

练习册系列答案
相关题目
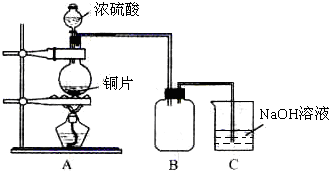
 某课外兴趣小组为探究铜跟浓硫酸的反应情况,设计了右图所示装置进行有关实验:
某课外兴趣小组为探究铜跟浓硫酸的反应情况,设计了右图所示装置进行有关实验: