题目内容
19世纪中叶,门捷列夫的突出贡献是( )
| A.提出原子学说 | B.发现元素周期律 |
| C.提出分子学说 | D.提出电离学说 |
B
解析试题分析:A、道尔顿提出了近代原子学说,错误;B、1869年,俄国化学家门捷列夫发现了元素周期律,正确;C、阿佛加德罗提出了分子学说,错误;D、阿伦尼乌斯提出电离学说,错误,答案选B。
考点:考查对化学史的掌握情况

练习册系列答案
相关题目
对充有氖气的霓虹灯管通电,灯管发出红色光。产生这一现象的主要原因( )
| A.在电流的作用下,氖原子与构成灯管的物质发生反应 |
| B.电子由基态向激发态跃迁时吸收除红光以外的光线 |
| C.氖原子获得电子后转变成发出红光的物质 |
| D.电子由激发态向基态跃迁时以光的形式释放能量 |
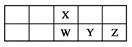
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法正确的是
| A.对应简单离子半径:X>W |
| B.对应气态氢化物的稳定性Y>Z |
| C.化合物XZW既含离子键,又含共价键 |
| D.Y的氧化物能与Z的氢化物和X的最高价氧化物对应的水化物的溶液反应 |
元素在周围表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期主族元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
已知16S、34Se位于同一主族,下列关系正确的是
| A.热稳定性:H2Se> H2S> HCl | B.原子半径:Se>P>Si |
| C.酸性:H3PO4>H2SO4>H2SeO4 | D.还原性:Se2->Br->Cl- |
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。已知Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )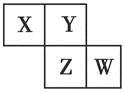
| A.原子半径:W>Z>Y>X |
| B.最高价氧化物对应水化物的酸性:Z>W>X |
| C.氢化物的稳定性:X>Y>Z |
| D.四种元素的单质中,Z单质的熔、沸点最高 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如右图所示,其中Z的核电荷数是Y的2倍。下列判断不正确的是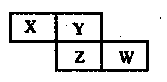
| A.最简单气态氢化物的热稳定性:Y>Z |
| B.最高价氧化物的水化物的酸性:X<W |
| C.X元素的氢化物与其最高价氧化物的水化物能形成离子化合物 |
| D.Y的氢化物沸点远高于Z的氢化物,是因为H-Y键的键能高于H-Z键的键能 |