题目内容
【题目】铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读图,下列判断不正确的是( ) 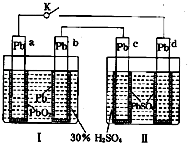
A.K闭合时,d电极反应式:PbSO4+2H2O﹣2e﹣=PbO2+4H++SO42﹣
B.当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2 mol
C.K闭合时,II中SO42﹣向c电极迁移
D.K闭合一段时间后,II可单独作为原电池,d电极为正极
【答案】C
【解析】解:A.K闭合时Ⅰ为原电池,Ⅱ为电解池,Ⅱ中发生充电反应,d电极为阳极发生氧化反应,其反应式为PbSO4+2H2O﹣2e﹣=PbO2+4H++SO42﹣ , 故A正确; B.在上述总反应式中,得失电子总数为2e﹣ , 当电路中转移0.2mol电子时,可以计算出Ⅰ中消耗的硫酸的量为0.2mol,故B正确;
C.K闭合时d是阳极,阴离子向阳极移动,故C错误;
D.K闭合一段时间,也就是充电一段时间后Ⅱ可以作为原电池,由于c表面生成Pb,放电时做电源的负极,d表面生成PbO2 , 做电源的正极,故D正确.
故选C.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目