题目内容
【题目】尼泊金酯是国际上公认的广谱性高效防腐剂,被广泛应用于食品、医药和化妆品的防腐等领域。我国国标规定,尼泊金酯中的乙酯、丙酯可用于食品。尼泊金丙酯(其相对分子质量约为180)在酸性条件下水解可生成两种有机物A和B。A的红外光谱表征到了羧基、羟基和苯环的存在,核磁共振氢谱表明其有4种不同化学环境的氢原子,且峰面积比为1:2:2:1。
(1)尼泊金丙酯中的含氧官能团的名称为________。
(2)为确定B的结构,可采用下列方法中的____________(填序号)。
a. 质谱法
b. 核磁共振氢谱法
c. 检验能否与NaHCO3溶液反应生成CO2
d. 检验能否发生氧化反应,并最终被氧化成羧酸
(3)写出A与足量NaOH溶液反应的化学方程式:________。
(4)尼泊金乙酯的同分异构体中,满足下列条件的共有___________种。
a. 分子中苯环上有两个对位取代基 b. 属于酯类 c. 可与浓溴水发生取代反应
写出这些同分异构体中,不含甲基的有机物的结构简式___________。
【答案】羟基和酯基 bd 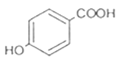 +2NaOH→
+2NaOH→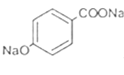 +2H2O 5
+2H2O 5 ![]()
【解析】
A的红外光谱表征到了羧基、羟基和苯环的存在,核磁共振氢谱表明其有4种不同化学环境的氢原子,且峰面积比为1:2:2:1,说明苯环取代基位于对位,且结构中无甲基、亚甲基存在,A的可能结构为HO-C6H4-COOH,相对分子质量为138,A和B酯化反应生成尼泊金丙酯,脱去一分子水,则B的相对分子质量为180+18-138=60,根据尼泊金丙酯名称可知,B有3个碳原子,不含羧基,即A在反应时脱去了羧基的-OH,酚羟基结构不变。
(1) A在反应时脱去了羧基的-OH,酚羟基结构不变,B脱去了羟基中的氢,尼泊金丙酯中的含氧官能团的名称为羟基和酯基。
(2)为确定B的结构,
a. 质谱法可得有机物相对分子质量,不能用于确定结构,A错误;
b. 核磁共振氢谱法可以判断氢环境,能用于确定有机物结构,B正确;
c. 检验能否与NaHCO3溶液反应生成CO2,若能反应,说明含有羧基,其余碳结构未知,C错误;
d. 检验能否发生氧化反应,并最终被氧化成羧酸,可得出羟基的位置和碳链结构,D正确;
答案为bd。
(3) A与足量NaOH溶液反应的化学方程式 +2NaOH→
+2NaOH→ +2H2O。
+2H2O。
(4)由上题可知,尼泊金乙酯为HO-C6H4-COOC2H5,,同分异构体中符合分子中苯环上有两个对位取代基的酯类,可与浓溴水发生取代反应的种类有5种,不含甲基的有机物的结构简式为![]() 。
。

【题目】(1)Al2(SO4)3溶液加热蒸干并灼烧最终得到物质是________________(填化学式),将NaHCO3与Al2(SO4)3两者溶液混合后可做泡沫灭火剂,其原理是_____________________(用离子方程式表示)
(2)实验室溶液中常用NaOH来进行洗气和提纯。当100mL 1mol·L-1的NaOH溶液吸收标准状况下2.24LSO2时,所得溶液中各离子浓度由大到小的顺序为____________________________
(3)25℃时,几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加NaOH溶液时,_____先沉淀(填离子符号),要使0.3mol·L-1硫酸铜溶液中Cu2+沉淀较为完全(当Cu2+浓度降至10-5 mol·L-1时),则应向溶液里加入氢氧化钠溶液使溶液pH为____(KspCu(OH)2=1×10-20)
【题目】中国传统文化中包括许多科技知识。下列古语中不涉及化学变化的是
千淘万漉虽辛苦,吹尽狂沙始到金 |
熬胆矾(CuSO4·5H2O) 铁釜,久之亦化为铜 |
凡石灰(CaCO3), 经火焚炼为用 |
丹砂(HgS)烧之成水银,积变又成丹砂 |
A | B | C | D |
A. A B. B C. C D. D
【题目】有机物A的相对分子质量不超过150, 经测定A具有下列性质:
A的性质 | 推断A的组成、结构 |
①能燃烧,燃烧产物只有CO2和H2O | __________ |
②A与醇或羧酸在浓硫酸存在下均能生成有香味的物质 | __________ |
③在一定条件下,A能发生分子内脱水反应,其生成物与溴水混合,溴水褪色 | |
④0.1 mol A与足量NaHCO3溶液反应产生4.48 L(标准状况下)气体 | ___________ |
(1)填写表中空白。
(2)若A分子中氧元素的质量分数为59.7%,则A的分子式为_______________
(3)若A分子中无含碳支链,写出反应③的化学方程式:_____________________。
(4)下列物质与A互为同系物的是________(填字母)。
a. ![]() b.
b. ![]()
c. ![]() d.
d. ![]()
【题目】已知化学反应①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其平衡常数为K2。在温度973 K和
FeO(s)+H2(g),其平衡常数为K2。在温度973 K和
1173 K情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1173 K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是________(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)![]() CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=_________。
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=_________。
(3)能判断反应③已达平衡状态的是_________。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(4)根据反应①与②可推导出K1、K2与K3之间的关系式_________。据此关系式及上表数据,也能推断出反应③是____________(填“吸热”或“放热”)反应。要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施是_______(填写序号)。
A.缩小反应容器容积 B.扩大反应容器容积
C.降低温度 D.升高温度
E.使用合适的催化剂 F.设法减少CO的量
【题目】下列有关实验的操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 实验结论 |
A | 向某溶液中加入硝酸酸化的BaCl2溶液 | 生成白色沉淀 | 原溶液中一定含有 |
B | 将 | 无白色沉淀生成 |
|
C | 向某溶液中加入少量双氧水后,再滴加几滴KSCN溶液 | 溶液变红色 | 原溶液中可能含有 |
D | 向某溶液中滴加稀盐酸 | 有气泡产生 | 原溶液中一定含有 |
A.AB.BC.CD.D