题目内容
【题目】把3molP和2.5molQ置于2L密闭容器中,发生如下反应:3P(g)+Q(g)![]() x M(g)+2N(g),5min后达到平衡生成1molN,经测定M的平均速率是0.1mol/(Lmin),下列叙述不正确的是
x M(g)+2N(g),5min后达到平衡生成1molN,经测定M的平均速率是0.1mol/(Lmin),下列叙述不正确的是
A.P的平均反应速率为0.15 mol/(Lmin)
B.Q的平衡浓度为1 mol/L
C.Q的转化率为25%
D.x等于2
【答案】C
【解析】
试题分析:A.已知达到平衡生成1molN,则参加反应的P为n(P)=3/2×1mol=1.5mol,所以v(P)=![]() =0.15 mol/(Lmin),A正确;B.已知达到平衡生成1molN,则参加反应的Q为n(Q)=1/2n(N)=0.5mol,所以Q的平衡浓度为:(2.5mol—0.5mol)÷2L=1 mol/L,B正确;C.参加反应的Q为n(Q)=1/2n(N)=0.5mol,故Q的转化率为
=0.15 mol/(Lmin),A正确;B.已知达到平衡生成1molN,则参加反应的Q为n(Q)=1/2n(N)=0.5mol,所以Q的平衡浓度为:(2.5mol—0.5mol)÷2L=1 mol/L,B正确;C.参加反应的Q为n(Q)=1/2n(N)=0.5mol,故Q的转化率为![]() ×100%=20%,C错误;D.根据A选项可知v(P)=0.15 mol/(Lmin),而M的平均速率是0.1mol/(Lmin),根据速率之比等于化学计量数之比可知x=2,D正确;答案选C。
×100%=20%,C错误;D.根据A选项可知v(P)=0.15 mol/(Lmin),而M的平均速率是0.1mol/(Lmin),根据速率之比等于化学计量数之比可知x=2,D正确;答案选C。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】已知在298K和101kPa条件下,有如下反应:
反应Ⅰ:C(s) + O2(g) = CO2(g) △ H1=-393.5 kJ·mol-1
反应Ⅱ:2C(s) + O2(g) = 2CO(g) △ H2=-221 kJ·mol-1
反应Ⅲ:N2(g) + O2(g) = 2NO(g) △ H3=+180.5 kJ·mol-1
试回答下列问题:
(1)汽车尾气净化原理为反应Ⅳ:2NO(g) + 2CO(g) ![]() N2(g) + 2CO2(g) △ H=______,该反应能自发进行的条件是_______。(填“高温”、“低温”或“任意温度”)。
N2(g) + 2CO2(g) △ H=______,该反应能自发进行的条件是_______。(填“高温”、“低温”或“任意温度”)。
(2)如果在一定温度下,体积为 2 升的密闭容器中发生化学反应Ⅳ,0~4min各物质物质的量的变化如下表所示:
物质(mol) 时间 | NO | CO | N2 | CO2 |
起始 | 0.40 | 1.0 | ||
2 min 末 | 2.0 | 0.80 | 1.6 | |
4 min 末 | 1.6 |
①求 0~2min 内用 CO 来表示的平均反应速率 v(CO)=________。
②试计算该温度下反应Ⅳ 的化学平衡常数 K=_________。
(3)若一定温度下,在容积可变的密闭容器中,上述反应Ⅳ达到平衡状态,此时容积为3L, c(N2)随时间 t 的变化曲线 x 如图所示。
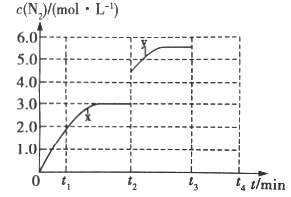
①若在 t2min时改变一个条件,c(N2)随反应时间 t 的变化如曲线 y 所示,则改变的条件是______。
②若在t2min时升高温度,t3min时重新达到平衡,请在图中画出在 t2~t4 内 c(N2)的变化曲线______。