题目内容
【题目】下列离子方程式正确的是( )
A. 钠与水反应:Na+H2O===Na++OH-+H2↑
B. 稀硫酸与氢氧化钡溶液反应:H++OH-===H2O
C. 铁与氯化铁溶液反应:Fe+Fe3+===2Fe2+
D. 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O===2A1O![]() +3H2↑
+3H2↑
【答案】D
【解析】A.钠与水反应,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故A错误;B.稀硫酸与氢氧化钡溶液反应,离子方程式:Ba2++SO42-+2H++2OH-═2H2O+BaSO4↓,故B错误;C.铁与氯化铁溶液反应,离子方程式:Fe+2Fe3+═3Fe2+,故C错误;D.铝与氢氧化钠溶液反应:2Al+2OH-+2H2O═2A1O2-+3H2↑,故D正确;故选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
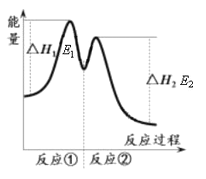
资料显示,反应分两步进行:① 2Fe3++H2O2 == 2Fe2++O2↑+2H+,② H2O2+2Fe2++2H+ == 2H2O+2Fe3+。反应过程中能量变化如下图所示。下列说法错误的是
A. Fe3+的作用是增大过氧化氢的分解速率
B. 反应①是吸热反应、反应②是放热反应
C. 反应2H2O2(aq) == 2H2O(l)+O2(g)的ΔH=E1-E2<0
D. 0~6 min的平均反应速率:v(H2O2)=3.33×10-2 mol·L-1·min-1

