题目内容
15.钮扣式银锌电池的电极分别是Zn 和 Ag2O,电解质溶液为KOH溶液,放电时电池反应式为:Zn+Ag2O+H2O═Zn(OH) 2+2Ag,负极材料是Zn,该电池放电时正极反应式为Ag2O+H2O+2e-═2Ag+2OH-.分析 电池反应式为:Zn+Ag2O+H2O═Zn(OH) 2+2Ag,根据化合价变化可知Zn被氧化,发生氧化反应,应为原电池的负极,则正极为Ag2O,得电子发生还原反应;
解答 解:由电池反应式为:Zn+Ag2O+H2O═Zn(OH) 2+2Ag,根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,得电子发生还原反应,则正极上发生反应:Ag2O+H2O+2e-═2Ag+2OH-,故答案为:Zn;Ag2O+H2O+2e-═2Ag+2OH-;
点评 本题考查原电池工作原理以及电极反应式的书写知识,题目难度不大,可以根据所学知识来回答.

练习册系列答案
相关题目
5.下列说法中,正确的是(NA代表阿伏加德罗常数)( )
| A. | 17 g氨气含有的原子总数为NA | |
| B. | 2.4 g金属镁与氧气完全反应时失去的电子数为0.1 NA | |
| C. | 常温常压下,6.4 g二氧化硫气体所含的氧原子数为0.2 NA | |
| D. | 常温常压下,11.2 L氯气含有的分子数为NA |
6.1.204×1024 个H2SO4分子的物质的量是( )
| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
3.国家电网表示促进新能发展和大范围优化配置,是电力工业科学发展的方向.下列关于能的说法中不正确的是( )
| A. | 发展核能发电,以减少火力发电带的SO2和CO2的排放问题 | |
| B. | 氢能是洁净的能,具有热值高、资丰富的优点 | |
| C. | 发展低碳经济,利用太阳能、风能实现城市照明 | |
| D. | 车用乙醇汽油具有提高燃油品质、无二氧化碳排放、燃烧充分等优点 |
10.用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 常温常压下,18gH2O中含有的原子总数为3NA | |
| C. | 标准状况下,0.1molCl2溶于水,转移的电子数目小于0.1NA | |
| D. | 常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA |
7.下列常见化合物的溶液中,滴人足量氨水最后仍为澄清溶液的是( )
| A. | 硫酸镁 | B. | 氯化铁 | C. | 氯化亚铁 | D. | 氯化铜 |
5.关于1mol•L-1 硫酸溶液,下列不正确的是( )
| A. | 1L该溶液中含溶质98g | |
| B. | 从10mL该溶液中取出5mL后,剩余溶液的浓度为1mol•L-1 | |
| C. | 将4.9g浓硫酸加入盛有50mL蒸馏水的烧杯中,充分溶解后就可配得该浓度的硫酸 | |
| D. | 该浓度的硫酸具有酸的通性,可与锌反应制取氢气 |
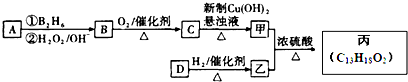
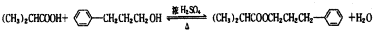 .
. .
.