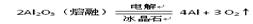题目内容
Ⅰ利用化学原理对工厂排放的废水、废渣等进行有效检测与合理处理。
(1)染料工业排放的废水中含有大量有毒的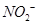 ,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去
,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去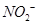 的离子方程式为_____________。
的离子方程式为_____________。
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(2)印刷电路铜板腐蚀剂常用FeCl3。腐蚀铜板后的混合浊液中,若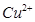 、
、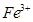 和
和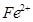 的浓度均为
的浓度均为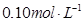 ,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中
,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中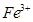 和
和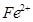 的实验步骤:①__________;②___________;③过滤。(提供的药品:C12、浓
的实验步骤:①__________;②___________;③过滤。(提供的药品:C12、浓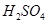 、NaOH溶液、CuO、Cu)。
、NaOH溶液、CuO、Cu)。
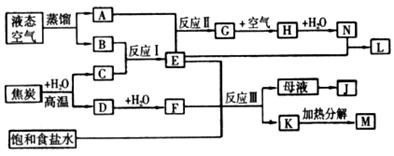
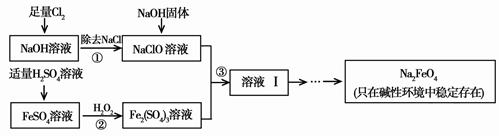
Ⅱ.下图表示某些化工生产的流程(部分反应条件和产物略去)
(1)反应Ⅰ需在500℃进行,其主要原因是_________________。
(2)G转化为H的过程中,需要不断补充空气,其原因是_________________。
(3)写出反应Ⅲ的化学方程式_________________。
(4)工业上,向析出K的母液中通氨气,加入细小食盐颗粒,冷却后可析出副产品。通入氨气的作用是_________________(填序号)。
a. 增大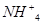 的浓度,使J更多地析出
的浓度,使J更多地析出
b. 使K更多地析出
c. 使K转化为M,提高析出的J的纯度
(5)写出上述流程所涉及的化学工业的名称_________________。
(1)染料工业排放的废水中含有大量有毒的
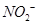 ,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去
,可以在碱性条件下加入铝粉除去(加热处理后的废水会产生能使湿润的红色石蕊试纸变蓝的气体)。除去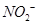 的离子方程式为_____________。
的离子方程式为_____________。常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | 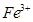 | 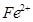 | 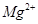 | 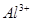 | 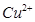 | 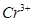 |
| 开始沉淀时的pH | 1.9 | 7.0 | — | — | 4.7 | — |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解) |
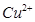 、
、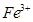 和
和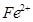 的浓度均为
的浓度均为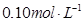 ,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中
,请参照上表给出的数据和提供的药品,简述除去CuCl2溶液中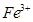 和
和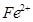 的实验步骤:①__________;②___________;③过滤。(提供的药品:C12、浓
的实验步骤:①__________;②___________;③过滤。(提供的药品:C12、浓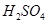 、NaOH溶液、CuO、Cu)。
、NaOH溶液、CuO、Cu)。Ⅱ.下图表示某些化工生产的流程(部分反应条件和产物略去)

(1)反应Ⅰ需在500℃进行,其主要原因是_________________。
(2)G转化为H的过程中,需要不断补充空气,其原因是_________________。
(3)写出反应Ⅲ的化学方程式_________________。
(4)工业上,向析出K的母液中通氨气,加入细小食盐颗粒,冷却后可析出副产品。通入氨气的作用是_________________(填序号)。
a. 增大
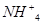 的浓度,使J更多地析出
的浓度,使J更多地析出b. 使K更多地析出
c. 使K转化为M,提高析出的J的纯度
(5)写出上述流程所涉及的化学工业的名称_________________。
Ⅰ. (6分,每空2分)(1)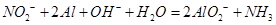 ↑
↑
(2)①向溶液中通入足量Cl2、②向溶液中加入CuO调节pH3.2-4.7
Ⅱ. (14分)(1)此温度下催化剂活性最高(2分)
(2)使NO不断转化为NO2提高原料利用率(3分)
(3)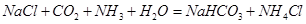 (3分) (4)ac(3分)
(3分) (4)ac(3分)
(5)合成氨工业 氨催化氧化制硝酸,侯德榜制碱法(3分)
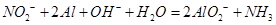 ↑
↑(2)①向溶液中通入足量Cl2、②向溶液中加入CuO调节pH3.2-4.7
Ⅱ. (14分)(1)此温度下催化剂活性最高(2分)
(2)使NO不断转化为NO2提高原料利用率(3分)
(3)
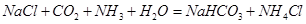 (3分) (4)ac(3分)
(3分) (4)ac(3分)(5)合成氨工业 氨催化氧化制硝酸,侯德榜制碱法(3分)
试题分析:Ⅰ.(1)加入铝粉后产生能使湿润的红色石蕊试纸变蓝的气体,这说明该气体应该是氨气。由于溶液显碱性,则铝被氧化生成AlO2-,所以该反应的离子方程式是NO2-+2Al+OH-+H2O=2AlO2-+NH3↑。
(2)由于亚铁离子开始沉淀时的pH大于铜离子开始沉淀时的pH值,所以应该首先通入氯气将亚铁离子氧化生成铁离子,然后加入氧化铜,通过控制溶液的pH在3.2~4.7之间即可除去铁离子。
Ⅱ. 液态空气蒸馏主要得到O2和N2,焦炭和水蒸气在高温下反应生成CO和H2,二者得到的气体B、C在催化剂条件下能发生反应,则应为N2和H2的反应,生成的气体为NH3,所以,A为O2,B为N2,C为H2,D为CO,E为NH3。NH3和O2在催化剂条件下发生氧化还原反应生成NO,NO与氧气反应生成NO2,进而与水反应生成硝酸和NO,所以G为NO,H为NO2,I为HNO3,L为NH4NO3。CO和O2反应生成CO2,CO2、NaCl和NH3反应生成NaHCO3,为侯氏制碱法的主要反应,NaHCO3加热分解生成Na2CO3,则F为CO2,J为NH4Cl,K为NaHCO3,M为Na2CO3。
(1)反应I是工业合成氨气的反应,需在500℃进行,其主要原因是此温度下催化剂活性最高。
(2)H转化为N的过程中是二氧化氮和水反应生成硝酸和一氧化氮的反应,反应是化学平衡,需要不断补充空气使一氧化氮气体不断转化为二氧化氮,提高原料的利用率。
(3)反应Ⅲ是候氏制碱法的反应原理,氨化的饱和食盐水中通入二氧化碳生成碳酸氢钠晶体和氯化铵,反应的化学方程式为NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl。
(4)工业上,向析出K的母液氯化铵中通氨气,加入细小食盐颗粒,冷却后可析出副产品J氯化铵,通入氨气的作用是增大铵根离子浓度使氯化铵晶体析出,氨气溶于水后生成氨水,氨水电离成铵根,增大铵根的浓度有利于氯化铵的析出;同时通入氨气使溶液碱性增强,使碳酸氢钠转化为溶解度较大的碳酸钠,可以提高氯化铵的纯度,故答案为ac。
(5)上述流程所涉及的化学工业的名称为:工业合成氨、氨气的催化氧化、侯德榜制碱法。
点评:该题是高考中的常见题型,属于中等难度的试题,对学生的要求高。试题综合性强,贴近高考,侧重对学生能力的培养和训练,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力以及动手操作能力。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。在进行无机物的推断时注意从空气的蒸馏和碳与水蒸气的反应入手,根据物质反应的条件作为突破口进行推断,学习中注意相关基础知识的积累、运用和总结。

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
 2Hg + O2 ↑
2Hg + O2 ↑