��Ŀ����
3������˵����ȷ���ǣ�������| A�� | ԭ�ӵĵ��Ӳ���Խ�࣬ԭ�Ӱ뾶һ��Խ�� | |
| B�� | ±��Ԫ�صĵ��ʾ��������ԣ�������۶���+7 | |
| C�� | ͬ��Ԫ������ԭ����������Ϊ16��26��36��46 | |
| D�� | ��A�����A��Ԫ�ؼ���γɹ��ۻ���������ӻ����� |
���� A��ԭ�Ӱ뾶�ɵ��Ӳ������˵���������ع�ͬ������
B����Ԫ��������õķǽ���Ԫ�أ������ۣ�
C��ͬ��Ԫ������ԭ����������Ϊ2��8��18��32�����������36��46��
D����A��Ԫ�ذ�����Ԫ�ء������Ԫ�أ���A��Ԫ��Ϊ���÷ǽ���Ԫ�أ�
��� �⣺A��ԭ�Ӻ˶Ժ�����ӵ�������������Ӷ࣬��Ӧ�ĺ���������Ҳ�࣬������������ǿӰ��ԭ�ӵİ뾶�����Ӳ�������ֻ��Ӱ��ԭ�Ӱ뾶������֮һ��ԭ�ӵ��Ӳ���Խ�࣬��Ӧ��ԭ�Ӱ뾶��һ������K��I��һ���Ӳ㣬���뾶K��I��A����
B����Ԫ��������õķǽ���Ԫ�أ�û�������ϼۣ���B����
C��ͬ��Ԫ������ԭ����������Ϊ2��8��18��32�����������36��46����C����
D����A��Ԫ�ذ�����Ԫ�ء������Ԫ�أ���A��Ԫ��Ϊ���÷ǽ���Ԫ�أ������γɹ��ۻ������ֿ����γ����ӻ������D��ȷ��
��ѡD��
���� ���⿼��ԭ�Ӻ�������Ų���Ϊ��Ƶ���㣬��Ŀ�ѶȲ�����ԭ�Ӻ�������Ų�����Ϊ���ؼ���������ػ���֪ʶ�Ŀ��飬������ѧ�������Ӧ��������

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
13�����й����л����˵����ȷ���ǣ�������
| A�� | ������������������������֮��Ϊ1��1 | |
| B�� | �ױ��ܷ����ӳɷ�Ӧ��������Ӧ��ȡ����Ӧ | |
| C�� | ����ϩ��ʹ����KMnO4��Һ����ˮ��ɫ��������ԭ����ͬ | |
| D�� |  ��C4H10�Ķ��ȴ������Ŀ��ͬ�����������칹�� ��C4H10�Ķ��ȴ������Ŀ��ͬ�����������칹�� |
14������̼ԭ�ӳɼ����ص㣬̼ԭ�ӿ������ϳ�̼����̼��������ΪC4H8���ܵ�ͬ���칹���У�������
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
11���������ӷ���ʽ��д��ȷ���ǣ�������
| A�� | �Ƹ�ˮ��Ӧ��Na+2H2O�TNa++2OH-+H2�� | |
| B�� | ϡ�������մ���Һ��Ӧ��HCO3-+H+�TCO2��+H2O | |
| C�� | ���θ�ʴ��·�壺2Fe3++Cu�T2Fe2++Cu2+ | |
| D�� | ���������Һ��ͨ�����������̼ Ca2++2ClO-+H2O+CO2�TCaCO3��+2HClO |
18�������йص������Һ������Ũ�ȹ�ϵ��ȷ���ǣ�������
| A�� | �� HCl �� CH3COONa ����Һ��Ϻ���Һ�����ԣ��� c��Na+ ����c��Cl- �� | |
| B�� | �� NH4Cl ��Һ��ͨ NH3���� c��NH4+ ����c��Cl- ����c��OH- ����c��H+ �� | |
| C�� | �����£�c��NH4+ ����ͬ�Ģ٣�NH4��2 CO3�ڣ�NH4��2 SO4 �ۣ�NH4��2 Fe��SO4��2��ҺŨ�ȴ�С˳��Ϊ���٣��ڣ��� | |
| D�� | ��֪ pKa=-lgKa��pKa��HF��=3.1��pKa��C6H5COOH��=4.2�������£����������Ũ�ȵ� NaF��C6H5COONa ��Һ�У�ǰ����������С�ں��� |
8�� ���ж���������Ԫ��X��Y��Z��R��T��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2 �����ӻ����Z��T�γɵ�Z2T���������ƻ�ˮ�ĵ���ƽ�⣮����Ԫ�ص�ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��ͼ��ʾ�������ƶϲ���ȷ���ǣ�������
���ж���������Ԫ��X��Y��Z��R��T��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2 �����ӻ����Z��T�γɵ�Z2T���������ƻ�ˮ�ĵ���ƽ�⣮����Ԫ�ص�ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��ͼ��ʾ�������ƶϲ���ȷ���ǣ�������
 ���ж���������Ԫ��X��Y��Z��R��T��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2 �����ӻ����Z��T�γɵ�Z2T���������ƻ�ˮ�ĵ���ƽ�⣮����Ԫ�ص�ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��ͼ��ʾ�������ƶϲ���ȷ���ǣ�������
���ж���������Ԫ��X��Y��Z��R��T��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2 �����ӻ����Z��T�γɵ�Z2T���������ƻ�ˮ�ĵ���ƽ�⣮����Ԫ�ص�ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��ͼ��ʾ�������ƶϲ���ȷ���ǣ�������| A�� | Y��Z��ɵĻ�����ֻ�����Ӽ� | |
| B�� | �⻯��ķе���ȶ�������R��Y | |
| C�� | ����������Ӧ��ˮ��������ԣ�T��R | |
| D�� | ��X��Y��Z��T����Ԫ����ɵĻ�����ˮ��Һһ�������� |
15�����й����������������ǣ�������
| A�� |  | B�� |  | ||
| C�� | 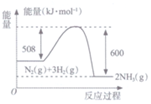 | D�� |  |
12������������ȷ���ǣ�������
| A�� | ���ȷ�Ӧ��ָ��Ӧ�������������������������� | |
| B�� | ���ȷ�Ӧ��ָ��Ӧ����ܼ��ܸ�����������ܼ��� | |
| C�� | �������������ͬ�ĵ�����ԭ�ӣ�һ����ͬ��Ԫ�ص�ԭ�� | |
| D�� | ����������ˮ��Ӧ���������ᣬ���Զ������������������� |
17�����й����л��������˵����ȷ���ǣ�������
| A�� | C2H4��C4H8һ����ͬϵ�� | |
| B�� | ����ϩ�;���ϩ���ܷ����ӳɷ�Ӧ | |
| C�� | C3H2Cl6��4��ͬ���칹�� | |
| D�� | ����������ϩ���Ҵ���ȫȼ����������������ͬ |