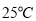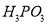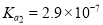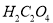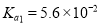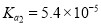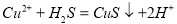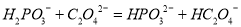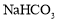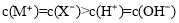جâؤ؟ؤعبف
£¨10·ض£©800،و،¢2Lأـ±صبفئ÷·´س¦2NO(g)£«O2(g) 2NO2(g)جهدµضذ£¬ n(NO)ثو
2NO2(g)جهدµضذ£¬ n(NO)ثو
ت±¼نµؤ±ن»¯بç±ي£؛
ت±¼ن£¨s£© | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
¼ئثم²¢»ط´ًدآءذختجâ£؛
£¨1£©·´س¦½ّذذµ½2 sت±c (NO)= ،£
£¨2£©سأO2±يت¾´س0،«2sؤع¸أ·´س¦µؤئ½¾ùثظآت¦ش£½___________،£
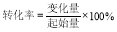 £¨3£© ·´س¦´ïµ½ئ½؛â×´ج¬ت±NOµؤ×ھ»¯آت= ،££¨جلت¾ £؛ £©
£¨3£© ·´س¦´ïµ½ئ½؛â×´ج¬ت±NOµؤ×ھ»¯آت= ،££¨جلت¾ £؛ £©
£¨4£©إذ¶دز»؟ةؤو·´س¦تا·ٌ´ïµ½ئ½؛â×´ج¬µؤزہ¾فسذ؛ـ¶à£¬ؤ³ح¬ر§صë¶ش¸أ·´س¦جل³ِز»ضضةèدë£؛²â¶¨بفئ÷ؤعئّجهµؤأـ¶ب£¬µ±أـ¶ب²»شظ¸ؤ±نت±¼´؟ةإذ¶د³ِ¸أ·´س¦زر¾´ïµ½ئ½؛â×´ج¬،£ؤمبدخھصâضضةèدëتا·ٌصب·£؟ £¨جî،°تا،±»ٍ،°·ٌ،±£©اëثµأ÷ؤمµؤہيسة ،£
(أ؟؟ص2·ض)
¢إ0.004mol/L£»¢ئ0.0015mol/(L?s)£»¢ا65%£»¢ب·ٌ ·´س¦خï،¢ةْ³ةخï¾ùخھئّجه£¬أـ±صبفئ÷ضذئّجهضتء؟؛حجه»²»±ن£¬ئّجهأـ¶بت¼ضص؛م¶¨،£
،¾½âخِ،؟
تشجâ·ضخِ£؛£¨1£©·´س¦½ّذذµ½2 sت±c (NO)=0.008mol،آ2L=0.004mol/L،£
£¨2£©سأO2±يت¾´س0،«2sؤع¸أ·´س¦µؤئ½¾ùثظآتv£½1/2،ء(0.020mol-0.008mol)،آ2L،آ2S=0.0015mol/(L?s)،£
£¨3£©·´س¦´ïµ½ئ½؛â×´ج¬ت±NOµؤ×ھ»¯آت=£¨0.020mol،ھ0.007mol£©،آ0.020mol،ء100%=65%،£
£¨4£©زٍخھ¸أ·´س¦µؤ·´س¦خï،¢ةْ³ةخï¾ùخھئّجه£¬¸ù¾فضتء؟تط؛م¶¨آةأـ±صبفئ÷ضذئّجهضتء؟²»±ن£¬أـ±صبفئ÷µؤجه»خھ2L£¬جه»²»±ن£¬ثùزشئّجهأـ¶بت¼ضص؛م¶¨£¬زٍ´ث²»ؤـ¸ù¾فأـ¶ب²»شظ¸ؤ±نت±إذ¶د³ِ¸أ·´س¦زر¾´ïµ½ئ½؛â×´ج¬،£
؟¼µم£؛±¾جâ؟¼²é»¯ر§·´س¦ثظآتءث؛ح×ھ»¯آتµؤ¼ئثم،¢»¯ر§ئ½؛â×´ج¬µؤإذ¶د،£

 جىجىدٍةدز»±¾؛أ¾يدµءذ´ً°¸
جىجىدٍةدز»±¾؛أ¾يدµءذ´ً°¸ ذ،ر§ةْ10·ضضسس¦سأجâدµءذ´ً°¸
ذ،ر§ةْ10·ضضسس¦سأجâدµءذ´ً°¸بثجهرھز؛ضذ´وشعئ½؛â£؛CO2 + H2O  H2CO3
H2CO3  HCO3،ھ £¬ت¹رھز؛pH±£³ضشع7.35~7.45ض®¼ن£¬·ٌشٍ¾ح»ل·¢ةْثلضذ¶¾»ٍ¼îضذ¶¾،£زرضھpHثوc(HCO3،ھ)©Uc(H2CO3) ±ن»¯¹طدµبçدآ±يثùت¾£¬شٍدآءذثµ·¨ضذ²»صب·µؤتا
HCO3،ھ £¬ت¹رھز؛pH±£³ضشع7.35~7.45ض®¼ن£¬·ٌشٍ¾ح»ل·¢ةْثلضذ¶¾»ٍ¼îضذ¶¾،£زرضھpHثوc(HCO3،ھ)©Uc(H2CO3) ±ن»¯¹طدµبçدآ±يثùت¾£¬شٍدآءذثµ·¨ضذ²»صب·µؤتا
c(HCO3،ھ)£؛c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
pH | 6.10 | 7.35 | 7.40 | 7.45 |
A£®pH=7µؤرھز؛ضذ£¬c(HCO3،ھ) > c(H2CO3)
B£®بثجه·¢ةْثلضذ¶¾ت±£¬؟ة¾²آِµخ×¢ز»¶¨إ¨¶بµؤNaHCO3بـز؛½â¶¾
C£®³£خآدآ½«pH=7.40µؤرھز؛د،تحضءpH=7ت±£¬c(H+)،¤c(OH،ھ)ز»¶¨²»±ن
D£®c(HCO3،ھ)©Uc(H2CO3)=1ت±£¬H2CO3µؤµçہë³ج¶بذ،سعHCO3،ھµؤث®½â³ج¶ب

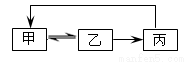
دآ±يضذ¸÷×éخïضتض®¼ن²»ؤـح¨¹ز»²½·´س¦تµدضسزح¼×ھ»¯µؤتا
| ¼× | زز | ±û |
A | CH2=CH2 | CH3CH2Cl | CH3CH2OH |
B | SiO2 | H2SiO3 | Na2SiO3 |
C | Cl2 | HCl | CuCl2 |
D | AlCl3 | Al(OH)3 | Al2O3 |