题目内容
A、B分别是碳原子数相同的烷烃和烯烃.现有2LA、B的混合气体在氧气中充分燃烧,生成8L二氧化碳和9.2L水蒸气(气体的体积均在同温同压下测定).
(1)试推测A与B的分子式;若有同分异构现象,写出烷烃A同分异构体的结构式.
(2)求混合气体中各组分的体积百分数.
(1)试推测A与B的分子式;若有同分异构现象,写出烷烃A同分异构体的结构式.
(2)求混合气体中各组分的体积百分数.
(1)体积之比等于物质的量之比,故n(有机物):n(CO2)=2L:8L=1:4,
根据C原子守恒可知,混合气体中平均分子组成中N(C)=4,
A、B分别是碳原子数相同的烷烃和烯烃,故分子中都含有4个C原子,故A为C4H10,B为C4H8,
C4H10的同分异构体的结构式有: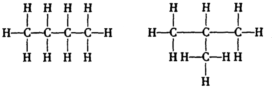 ,
,
答:A为C4H10,B为C4H8;A的同分异构体有 .
.
(2)体积之比等于物质的量之比,故n(有机物):n(H2O)=2L:9.2L=1:4.6,
根据C原子守恒可知,混合气体中平均分子组成中N(H)=
=9.2,
令A为C4H10的体积分数为x,则C4H8的体积分数为1-x,根据平均H原子数目有:
10x+8(1-x)=9.2,
解得x=0.6
故C4H8的体积分数为1-x=1-0.6=0.4,
答:C4H10的体积分数为0.6,C4H8的体积分数为0.4.
根据C原子守恒可知,混合气体中平均分子组成中N(C)=4,
A、B分别是碳原子数相同的烷烃和烯烃,故分子中都含有4个C原子,故A为C4H10,B为C4H8,
C4H10的同分异构体的结构式有:
 ,
,答:A为C4H10,B为C4H8;A的同分异构体有
 .
.(2)体积之比等于物质的量之比,故n(有机物):n(H2O)=2L:9.2L=1:4.6,
根据C原子守恒可知,混合气体中平均分子组成中N(H)=
| 4.6×1 |
| 1 |
令A为C4H10的体积分数为x,则C4H8的体积分数为1-x,根据平均H原子数目有:
10x+8(1-x)=9.2,
解得x=0.6
故C4H8的体积分数为1-x=1-0.6=0.4,
答:C4H10的体积分数为0.6,C4H8的体积分数为0.4.

练习册系列答案
相关题目
(10分)800℃、2L密闭容器反应2NO(g)+O2(g) 2NO2(g)体系中, n(NO)随
2NO2(g)体系中, n(NO)随
时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
计算并回答下列问题:
(1)反应进行到2 s时c (NO)= 。
(2)用O2表示从0~2s内该反应的平均速率υ=___________。
 (3) 反应达到平衡状态时NO的转化率= 。(提示 : )
(3) 反应达到平衡状态时NO的转化率= 。(提示 : )
(4)判断一可逆反应是否达到平衡状态的依据有很多,某同学针对该反应提出一种设想:测定容器内气体的密度,当密度不再改变时即可判断出该反应已经达到平衡状态。你认为这种设想是否正确? (填“是”或“否”)请说明你的理由 。

