题目内容
【题目】ClO2是一种优良的消毒剂,其溶解度约是Cl2的5倍,但温度过高、浓度过大时均易发生分解,因此常将其制成固体,以便运输和贮存。制备KClO2固体的实验裝置如图所示,其中A装置制备ClO2,B装置制备KClO2。请回答下列问题:
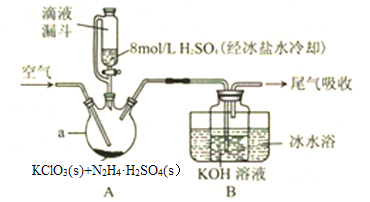
(1)仪器a的名称是________。
(2)滴液漏斗与普通分液漏斗相比,其优点是_________。
(3)加入的硫酸需要用冰盐水冷却的原因是_________。
(4)实验过程中通入空气的目的是________,空气流速过快或过慢,均降低KClO2产率,试解释其原因________ 。
(5)用图示装置制备的KClO2中含有较多杂质,其原因是________。
(6)A中制备ClO2的化学方程式为_________ 。
(7)有人认为用图示装置吸收ClO2易引起倒吸,但经过多次实验均未发现有倒吸现象,其原因是________。
【答案】 三颈烧瓶 滴液漏斗液面上方和三颈烧瓶液面上方气压相等,使液体能順利滴下 防止液体飞溅,防止生成的ClO2分解 将生成的ClO2全部赶出以被KOH吸收 空气流速过慢时,ClO2不能及时被移走,浓度过高会导致分解;空气流速过快吋,ClO2不能被充分吸收 生成KClO2的同吋必有ClO2的氧化产物KClO3或KClO4 4 KClO2+N2H4·H2SO4+H2SO4=4ClO2+N2↑+2K2SO4+4H2O(K2SO4写成KHSO4也可以) 生成ClO2的同时也产生N2,或有持续通入的空气流
【解析】(1)仪器a为反应的发生器,是三颈烧瓶;正确答案:三颈烧瓶。
(2)滴液漏斗与普通分液漏斗相比,其优点是滴液漏斗液面上方和三颈烧瓶液面上方气压相等,使液体能順利滴下;正确答案:滴液漏斗液面上方和三颈烧瓶液面上方气压相等,使液体能順利滴下。
(3)浓硫酸溶于水放出大量的热,会导致反应生成的ClO2分解,产率降低,同时也能防止浓硫酸稀释时液体飞溅;因此加入的硫酸需要用冰盐水冷却;正确答案:防止液体飞溅,防止生成的ClO2分解。
(4)实验过程中通入空气的目的是能够使反应产生的ClO2全部被氢氧化钾溶液吸收,提高ClO2的利用率,但如果空气流速过快或过慢,均降低KClO2产率;其原因是空气流速过慢时,ClO2不能及时被移走,浓度过高会导致分解;空气流速过快吋,ClO2不能被充分吸收;正确答案:将生成的ClO2全部赶出以被KOH吸收; 空气流速过慢时,ClO2不能及时被移走,浓度过高会导致分解;空气流速过快吋,ClO2不能被充分吸收。
(5)用图示装置制备的KClO2中含有较多杂质,根据氧化还原反应规律,ClO2与碱反应时,生成KClO2的同吋,必有ClO2的氧化产物KClO3或KClO4 生成;正确答案:生成KClO2的同吋必有ClO2的氧化产物KClO3或KClO4。
(6)根据题给信息可知:KClO2与N2H4·H2SO4在酸性条件下反应生成ClO2和氮气等物质,化学方程式为4KClO2+N2H4·H2SO4+H2SO4=4ClO2+N2↑+2K2SO4+4H2O;正确答案:4KClO2+N2H4·H2SO4+H2SO4=4ClO2+N2↑+2K2SO4+4H2O(K2SO4写成KHSO4也可以)。
(7)反应生成ClO2的同时,还产生N2,同时该反应过程中有持续通入的空气流,因此不能产生倒吸现象;正确答案:生成ClO2的同时也产生N2,或有持续通入的空气流。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案