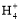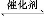МвДҝДЪИЭ
ТСЦӘҙЧЛбәНСОЛбКЗИХіЈЙъ»оЦРј«ОӘіЈјыөДЛб,ФЪТ»¶ЁМхјюПВ,CH3COOHИЬТәЦРҙжФЪөзАлЖҪәв:CH3COOH CH3COO-+H+ЎЎҰӨH>0ЎЈ
CH3COO-+H+ЎЎҰӨH>0ЎЈ
(1)іЈОВПВ,ФЪpH=5өДПЎҙЧЛбИЬТәЦР,c(CH3COO-)=ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(БРКҪ,І»ұШ»Ҝјт);ПВБР·Ҫ·ЁЦР,ҝЙТФК№0.10 molЎӨL-1 CH3COOHөДөзАліМ¶ИФцҙуөДКЗЎЎЎЎЎЎЎЎ ЎЈ
a.јУИлЙЩБҝ0.10 molЎӨL-1өДПЎСОЛб
b.јУИИCH3COOHИЬТә
c.јУЛ®ПЎКНЦБ0.010 molЎӨL-1
d.јУИлЙЩБҝұщҙЧЛб
e.јУИлЙЩБҝВИ»ҜДЖ№ММе
f.јУИлЙЩБҝ0.10 molЎӨL-1өДNaOHИЬТә
(2)Ҫ«өИЦКБҝөДРҝН¶ИлөИМе»эЗТpHҫщөИУЪ3өДҙЧЛбәНСОЛбИЬТәЦР,ҫӯ№эід·Ц·ҙУҰәу,·ўПЦЦ»ФЪТ»ЦЦИЬТәЦРУРРҝ·ЫКЈУа,ФтЙъіЙЗвЖшөДМе»э:V(СОЛб)ЎЎЎЎЎЎЎЎV(ҙЧЛб),·ҙУҰөДЧоіхЛЩВКОӘ:v(СОЛб)ЎЎЎЎЎЎЎЎv(ҙЧЛб)(МоЎ°>ЎұЎўЎ°<Ўұ»тЎ°=Ўұ)ЎЈ
(3)іЈОВПВ,ПтМе»эОӘVa mL,pHОӘ3өДҙЧЛбИЬТәЦРөОјУpH=11өДNaOHИЬТәVb mLЦБИЬТәЗЎәГіКЦРРФ,ФтVaУлVbөД№ШПөКЗЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
(4)іЈОВПВ,Ҫ«0.1 mol/LСОЛбәН0.1 mol/LҙЧЛбДЖИЬТә»мәП,ЛщөГИЬТәОӘЦРРФ,Фт»мәПИЬТәЦРёчАлЧУөДЕЁ¶И°ҙУЙҙуөҪРЎЕЕРтОӘЎЎ ЎЈ
(5)ТСЦӘ:90 ЎжКұ,Л®өДАлЧУ»эіЈКэОӘKW=3.8ЎБ10-13,ФЪҙЛОВ¶ИПВ,Ҫ«pH=3өДСОЛбәНpH=11өДЗвСх»ҜДЖИЬТәөИМе»э»мәП,Фт»мәПИЬТәЦРөДc(H+)=ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(ұЈБфИэО»УРР§КэЧЦ) mol/LЎЈ
(1)(10-5-10-9) mol/LЎЎbcf
(2)<ЎЎ=ЎЎ(3)Va<Vb
(4)c(Na+)>c(CH3COO-)>c(Cl-)>c(H+)=c(OH-)
(5)2.05ЎБ10-11
ЎҫҪвОцЎҝ(1)ФЪpH=5өДПЎҙЧЛбИЬТәЦР,c(H+)=10-5 mol/L,ёщҫЭЛ®өДөзАлЖҪәвј°ҙЧЛбөДөзАлЖҪәв·ҪіМКҪCH3COOH H++CH3COO-ҝЙТФҝҙіц,c(CH3COO-)=c(H+)ИЬТә-c(H+)Л®=(10-5-10-9) mol/L;јУИИЎўјУЛ®ПЎКНЎўјУИлјоРФОпЦКҫщДЬК№өзАлЖҪәвПтУТТЖ¶Ҝ,№КСЎbcfЎЈ
H++CH3COO-ҝЙТФҝҙіц,c(CH3COO-)=c(H+)ИЬТә-c(H+)Л®=(10-5-10-9) mol/L;јУИИЎўјУЛ®ПЎКНЎўјУИлјоРФОпЦКҫщДЬК№өзАлЖҪәвПтУТТЖ¶Ҝ,№КСЎbcfЎЈ
(2)ҙЧЛбКЗИхЛб,өИМе»эөИpH,Фтn(CH3COOH)>n(HCl),ФтСОЛбЦРРҝ·ЫКЈУа,ЛжЧЕЛьәНҪрКфөД·ҙУҰ,өзАлЖҪәвІ»¶ПөШПтУТТЖ¶Ҝ,»бөзАліцёь¶аөДЗвАлЧУ,ЛщТФҙЧЛбІъЙъөДЗвЖшМе»эҪПҙу,ҝӘКјКұ,ҙЧЛбәНСОЛбөДpHҫщөИУЪ3,јҙҝӘКјКұЗвАлЧУөДЕЁ¶ИПаөИ,ЛщТФҝӘКјКұөДЛЩВКПаөИЎЈ
(3)ҙЧЛбКЗИхЛб,pHОӘ3өДҙЧЛбИЬТәЦР,CH3COOHөДЕЁ¶ИҙуУЪ10-3 mol/L,pH=11өДNaOHИЬТәЕЁ¶ИөИУЪ10-3 mol/L,ЧоәуИЬТәЗЎәГіКЦРРФ,ЛөГчјо№эБҝ,ЛщТФVa<VbЎЈ
(4)ёщҫЭөзәЙКШәг:c(CH3COO-)+c(Cl-)+c(OH-)=c(Na+)+c(H+),ИЬТәОӘЦРРФ,ҝЙТФЦӘөАc(CH3COO-)+c(Cl-)=c(Na+),ЛщТФc(Na+)>c(CH3COO-)>c(Cl-)>c(H+)=c(OH-)ЎЈ
(5)pH=3өДСОЛбЦРc(H+)=10-3 mol/L,pH=11өДЗвСх»ҜДЖИЬТәЦР:c(OH-)= =38ЎБ10-3 mol/L,»мәПәујоКЈУа,КЈУаөДЗвСхёщөДЕЁ¶ИОӘ:c(OH-)=
=38ЎБ10-3 mol/L,»мәПәујоКЈУа,КЈУаөДЗвСхёщөДЕЁ¶ИОӘ:c(OH-)= =0.018 5 mol/L,
=0.018 5 mol/L,
ЛщТФc(H+)= mol/LЎЦ2.05ЎБ10-11 mol/LЎЈ
mol/LЎЦ2.05ЎБ10-11 mol/LЎЈ

 ГыРЈҝОМГПөБРҙр°ё
ГыРЈҝОМГПөБРҙр°ё°ұКЗөӘСӯ»·№эіМЦРөДЦШТӘОпЦК,°ұөДәПіЙКЗДҝЗ°ЖХұйК№УГөДИЛ№Ө№МөӘ·Ҫ·ЁЎЈ
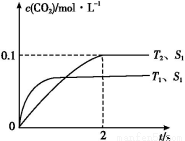
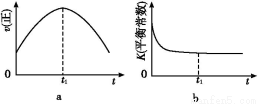
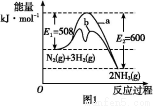
(1)ёщҫЭНј1МṩөДРЕПў,РҙіцёГ·ҙУҰөДИИ»ҜС§·ҪіМКҪ:ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ,ФЪНј1ЦРЗъПЯЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(МоЎ°aЎұ»тЎ°bЎұ)ұнКҫјУИлМъҙҘГҪөДДЬБҝұд»ҜЗъПЯЎЈ
(2)ФЪәгИЭИЭЖчЦР,ПВБРГиКцЦРДЬЛөГчЙПКц·ҙУҰТСҙпЖҪәвөДКЗЎЎЎЎЎЎЎЎЎЈ
A.3v(H2)Хэ=2v(NH3)Дж
B.өҘО»КұјдДЪЙъіЙn mol N2өДН¬КұЙъіЙ2n mol NH3
C.»мәПЖшМеөДГЬ¶ИІ»ФЩёДұд
D.ИЭЖчДЪС№ЗҝІ»ЛжКұјдөДұд»Ҝ¶шұд»Ҝ
(3)Т»¶ЁОВ¶ИПВ,Пт2 LГЬұХИЭЖчЦРідИл1 mol N2әН3 mol H2,ұЈіЦМе»эІ»ұд,0.5 minәуҙпөҪЖҪәв,ІвөГИЭЖчЦРУР0.4 mol NH3,ФтЖҪҫщ·ҙУҰЛЩВКv(N2)=ЎЎЎЎЎЎЎЎЎЎЎЎ,ёГОВ¶ИПВөДЖҪәвіЈКэK=ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈИфЙэёЯОВ¶И,KЦөұд»ҜЎЎЎЎЎЎЎЎ(МоЎ°ФцҙуЎұЎўЎ°јхРЎЎұ»тЎ°І»ұдЎұ)ЎЈ
(4)ОӘБЛС°ХТәПіЙNH3өДОВ¶ИәНС№ЗҝөДККТЛМхјю,ДіН¬С§ЙијЖБЛИэЧйКөСй,Іҝ·ЦКөСйМхјюТСҫӯМоФЪПВГжКөСйЙијЖұнЦРЎЈ
КөСйұаәЕ | T(Ўж) | n(N2)/n(H2) | p(MPa) |
ўЎ | 450 | 1/3 | 1 |
ўў | ЎЎ | ЎЎ | 10 |
ўЈ | 480 | ЎЎ | 10 |
A.ЗлФЪЙПұнҝХёсЦРМоИлКЈУаөДКөСйМхјюКэҫЭЎЈ
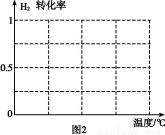
B.ёщҫЭ·ҙУҰN2(g)+3H2(g) 2NH3(g)өДМШөг,ФЪёшіцөДЧшұкНј2ЦР,»ӯіцЖдФЪ1 MPaәН10 MPaМхјюПВH2өДЧӘ»ҜВКЛжОВ¶Иұд»ҜөДЗчКЖЗъПЯКҫТвНј,ІўұкГчёчМхЗъПЯөДС№ЗҝЎЈ
2NH3(g)өДМШөг,ФЪёшіцөДЧшұкНј2ЦР,»ӯіцЖдФЪ1 MPaәН10 MPaМхјюПВH2өДЧӘ»ҜВКЛжОВ¶Иұд»ҜөДЗчКЖЗъПЯКҫТвНј,ІўұкГчёчМхЗъПЯөДС№ЗҝЎЈ
өз¶ЖОЫДаЦРә¬УРCr(OH)3ЎўAl2O3ЎўZnOЎўCuOЎўNiOөИОпЦК,№ӨТөЙПНЁ№эЎ°ЦРОВұәЙХЎӘДЖСх»Ҝ·ЁЎұ»ШКХNa2Cr2O7өИОпЦКЎЈ

ТСЦӘ:ФЪNa2CrO4ИЬТәЦРә¬УРЙЩБҝNaAlO2ЎўNa2ZnO2өИОпЦК
(1)Л®ҪюәуөДИЬТәіКЎЎЎЎЎЎЎЎРФ(МоЎ°ЛбЎұЎўЎ°јоЎұ»тЎ°ЦРЎұ)ЎЈ
(2)НкіЙСх»ҜұәЙХ№эіМЦРЙъіЙNa2CrO4өД»ҜС§·ҪіМКҪЎЈ
ЎЎЎЎЎЎЎЎCr(OH)3+ЎЎЎЎЎЎЎЎNa2CO3+ЎЎЎЎЎЎЎЎЎЎЎЎ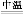 ЎЎЎЎЎЎЎЎNa2CrO4+ЎЎЎЎЎЎЎЎCO2+ЎЎЎЎЎЎЎЎЎЎЎЎ
ЎЎЎЎЎЎЎЎNa2CrO4+ЎЎЎЎЎЎЎЎCO2+ЎЎЎЎЎЎЎЎЎЎЎЎ
(3)ВЛФьўтөДЦчТӘіЙ·ЦУРZn(OH)2ЎўЎЎЎЎЎЎЎЎЎЈ
(4)Ў°ПөБРІЩЧчЎұЦРОӘ:јМРшјУИлH2SO4,ЎЎЎЎЎЎЎЎ,АдИҙҪбҫ§,№эВЛЎЈјМРшјУИлH2SO4ДҝөДКЗЎЎ ЎЈ
ТСЦӘ:ўЩіэИҘВЛФьIIәу,ИЬТәЦРҙжФЪИзПВ·ҙУҰ:
2CrO42ЎӘ+2H+ Cr2O72ЎӘ+H2O
Cr2O72ЎӘ+H2O
ўЪNa2Cr2O7ЎўNa2CrO4ФЪІ»Н¬ОВ¶ИПВөДИЬҪв¶ИИзПВұн
ОВ¶И ИЬҪв¶И »ҜС§КҪ | 20 Ўж | 60 Ўж | 100 Ўж |
Na2SO4 | 19.5 | 45.3 | 42.5 |
Na2Cr2O7 | 183 | 269 | 415 |
Na2CrO4 | 84 | 115 | 126 |
(5)№ӨТөЙП»№ҝЙТФФЪЛ®Ҫю№эВЛәуөДИЬТә(Na2CrO4)јУИлККБҝH2SO4,УГКҜД«Ччөзј«өзҪвЙъІъҪрКфёх,РҙіцЙъіЙёхөДөзј«·ҙУҰ·ҪіМКҪЎЎ ЎЈ