题目内容
下列微粒中,其核外电子数相同( )
①13Al3+②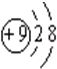 ③
③ ④F-.
④F-.
①13Al3+②
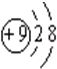 ③
③ ④F-.
④F-.| A、①②③ | B、②③④ |
| C、①②④ | D、①③④ |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:原子变成阴离子时电子层数不变,原子变成阳离子时电子层数减少一个,同一周期的阴阳离子电子层数不同,同一周期的阴离子和下一周期的阳离子电子层结构相同,其核外电子数相同,据此分析解答.
解答:
解:①13Al3+核外电子数为10;
②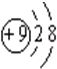 核外电子数为10;
核外电子数为10;
③ 核外电子数为18;
核外电子数为18;
④F-核外电子数为10;
所以核外电子数相同的为①②④.
故选C.
②
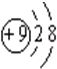 核外电子数为10;
核外电子数为10;③
 核外电子数为18;
核外电子数为18;④F-核外电子数为10;
所以核外电子数相同的为①②④.
故选C.
点评:本题考查了阴阳离子、原子的电子层结构,难度不大,明确阴阳离子中核外电子数的计算方法是解本题的关键.

练习册系列答案
相关题目
天宫一号搭载的长征二号火箭使用的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R+2N2O4=3N2+4H2O+2CO2,下列叙述错误的
是( )
是( )
| A、此反应中R的分子式为C2H8N2 |
| B、此反应是氧化还原反应,N2O4做氧化剂 |
| C、每生成67.2L N2转移电子数为8NA |
| D、此反应可在瞬间产生大量高温气体,推动火箭飞行 |
常温下,在溶液中可发生以下反应:①2Fe2++Br2=2Fe3++2Br- ②2Br-+Cl2=Br2+2Cl- ③2Fe3++2I-=2Fe2++I2.由此判断下列说法正确的是( )
| A、铁元素在反应①中被还原,在③中被氧化 |
| B、反应②中当有1mol Cl2被氧化时,有2mol Br-被还原 |
| C、氧化性强弱顺序为:Cl2>I2>Br2>Fe3+ |
| D、还原性强弱顺序为:I->Fe2+>Br->Cl- |
已知相同条件下,HClO的电离常数小于H2CO3的第一级电离常数(Ka1)大于H2CO3的第二级电离常数(Ka2).为了提高氯水中HClO的浓度,可行的是( )
| A、通入HCl(g) |
| B、加入NaHCO3(s) |
| C、加入H2O |
| D、加入NaOH(s) |
将金属钠分别投入下列物质的水溶液中,产生气体和蓝色沉淀的是( )
| A、NaCl |
| B、K2SO4 |
| C、CuCl2 |
| D、MgCl2 |
常温下,对于①0.1mol/L CH3COOH溶液 ②pH=1HCl溶液 ③pH=13的NaOH溶液 ④0.1mol/L CH3COONa溶液,下列说法正确的是( )
| A、①和②分别稀释100倍后的pH:②>① | ||
| B、水电离出的c(OH-):④>③>①>② | ||
C、①和③混合后溶液呈中性:
| ||
D、①和④混合后溶液呈酸性:
|
关于溶液的下列说法正确的是( )
| A、用湿润的pH试纸测稀碱液的pH,测定值偏大 |
| B、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
| C、已知:H2B?H++HB-,HB-?H++B2-(电离常数K1=1.3×10-7,K2=7.1×10-15),则NaHB溶液显酸性 |
| D、除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
将①氢气;②氧气;③甲烷三种气体分别盛放在三个容器中,并保持三个容器内气体的温度和密度均相等,这三种气体压强的大小关系是( )
| A、①>②=③ |
| B、①>③>② |
| C、①<②<③ |
| D、①<③<② |