题目内容
【题目】某校化学兴趣小组制备消毒液(主要成分是NaClO),设计了下列装置。
已知:Cl2和NaOH溶液能发生下列反应
在加热时:![]()
在低温时:![]()
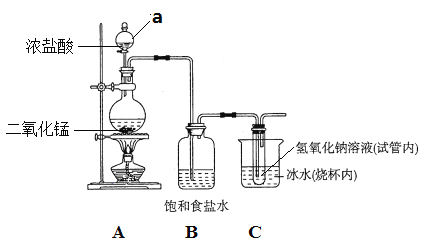
试回答下列问题:
⑴仪器a的名称是_____________。
⑵连接好装置,装药品之前,必须进行的一项操作是_________________。
⑶A装置内发生反应的化学方程式为_______________________________。
⑷B的作用是___________;冰水的作用是__________________________。
⑸该装置的不足之处有___________________________________________。
⑹一定温度下,向NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中含有三种含氯元素的离子,其中ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
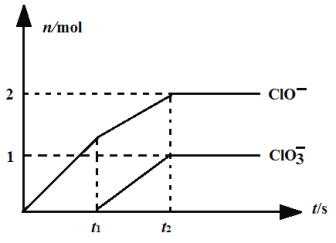
该过程中t2时刻参加反应的Cl2物质的量为_________mol;若另一过程产生的n(Cl-)为5.5mol,n(ClO3-)为1mol,则参加反应的NaOH物质的量为___________________mol。
【答案】分液漏斗 检查实验装置气密性 MnO2 +4HCl(浓)![]() MnCl2 + Cl2↑ +2H2O 除去氯气中的HCl 防止溶液温度升高发生副反应生成NaClO3,降低了产品的产率 没有尾气吸收处理装置 5 7
MnCl2 + Cl2↑ +2H2O 除去氯气中的HCl 防止溶液温度升高发生副反应生成NaClO3,降低了产品的产率 没有尾气吸收处理装置 5 7
【解析】
本题是一道以氯气及其化合物为核心的氧化还原题目,难度一般。
(1)仪器a有塞子和开关,为分液漏斗;
(2)在连接好装置后一定要先检查装置的气密性,若气密性不好则不能继续进行实验;
(3)A装置内发生的就是实验室制氯气的反应,写出方程式即可:![]() ;
;
(4)B中的饱和食盐水可以吸收氯化氢,但是不吸收氯气,因此可以起到除去氯气中的氯化氢的作用;而冰水是为了给![]() 溶液降温,防止溶液温度过高产生氯酸钠等副产物;
溶液降温,防止溶液温度过高产生氯酸钠等副产物;
(5)该装置没有尾气处理装置,而氯气是有毒的,因此需要加一个尾气处理装置;
(6)首先这是一个氯气的歧化反应,因此有![]() 这样一个关系存在,保证反应中得失的电子数一致;而当t2时
这样一个关系存在,保证反应中得失的电子数一致;而当t2时![]() 为2mol,
为2mol,![]() 为1mol,代入关系式解得
为1mol,代入关系式解得![]() 为7mol,因此氯元素一共有10mol,这些氯元素全部是氯气中的,则参加反应的氯气一共有5mol;第二问里代入
为7mol,因此氯元素一共有10mol,这些氯元素全部是氯气中的,则参加反应的氯气一共有5mol;第二问里代入![]() 和
和![]() 的物质的量解出
的物质的量解出![]() 的物质的量为0.5mol,不管是
的物质的量为0.5mol,不管是![]() 、
、![]() 还是
还是![]() ,钠和氯都是1:1的,因此氯一共有7mol,钠也一共有7mol,参加反应的
,钠和氯都是1:1的,因此氯一共有7mol,钠也一共有7mol,参加反应的![]() 也是7mol。
也是7mol。