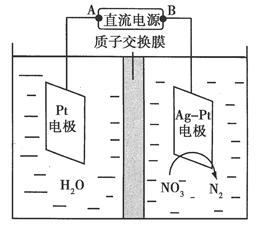
题目内容
已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
Cu+2H2SO4(浓)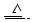 CuSO4+A↑+2H2O
CuSO4+A↑+2H2O
试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成。则A应该属于 (用字母代号填写)
A.酸 B.碱 C.盐 D.酸性氧化物 E.碱性氧化物
A物质可以使酸性KMnO4溶液褪色,此反应中 (填写化学式,下同)失去电子,氧化剂是 。
(2)若A物质通入品红溶液,观察到溶液褪色,说明A物质具有 (填序号,下同);若A物质通入Na2S溶液,观察到溶液中出现淡黄色浑浊,说明SO2具有 。
A.氧化性 B.还原性 C.漂白性
若A物质通入双氧水,请大胆判断所得溶液是 (填溶质的化学式)
(3)一定量的铜片与100mL 18mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的A气体在标准状况下体积为 L (假设气体全部逸出)。若用4 mol·L-1的NaOH溶液吸收生成的A,并生成正盐,写出发生的反应方程式 计算需要NaOH溶液的体积 L。
(1)D;SO2;KMnO4 (2)C;A;H2SO4。
(3)2.24;2NaOH + SO2 =Na2SO3 + H2O;0.05
解析试题分析:(1)铜和浓硫酸反应的化学方程式为Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O。SO2属于酸性氧化物。因此选项为D。SO2可以使酸性KMnO4溶液褪色,是由于发生反应:2KMnO4+ 5SO2+2H2O=K2SO4+2MnSO4+2H2SO4。在此反应中,SO2失去电子,作还原剂;KMnO4得到电子,作氧化剂,表现氧化性。(2)若SO2通入品红溶液,观察到溶液褪色,是因为SO2有漂白性。若A物质通入Na2S溶液,观察到溶液中出现淡黄色浑浊,是因为发生反应:SO2+H2O=H2SO3. H2SO3+Na2S=Na2SO3+H2S;SO2+2H2S="3S↓+" 2H2O. 说明SO2具有氧化性。若将SO2通入双氧水中,则发生氧化还原反应:SO2+H2O2=H2SO4,产生硫酸。(3)铜和浓硫酸反应的化学方程式为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O。SO2属于酸性氧化物。因此选项为D。SO2可以使酸性KMnO4溶液褪色,是由于发生反应:2KMnO4+ 5SO2+2H2O=K2SO4+2MnSO4+2H2SO4。在此反应中,SO2失去电子,作还原剂;KMnO4得到电子,作氧化剂,表现氧化性。(2)若SO2通入品红溶液,观察到溶液褪色,是因为SO2有漂白性。若A物质通入Na2S溶液,观察到溶液中出现淡黄色浑浊,是因为发生反应:SO2+H2O=H2SO3. H2SO3+Na2S=Na2SO3+H2S;SO2+2H2S="3S↓+" 2H2O. 说明SO2具有氧化性。若将SO2通入双氧水中,则发生氧化还原反应:SO2+H2O2=H2SO4,产生硫酸。(3)铜和浓硫酸反应的化学方程式为Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,在反应方程式中,每产生1mol的SO2气体,电子转移2mol.。现在电子转移了0.2mol,所以产生了0.1mol的SO2气体。在标准状况下,其体积为2.24L。若用4 mol·L-1的NaOH溶液吸收生成的SO2,并生成正盐,则该反应的反应方程式为2NaOH + SO2 =Na2SO3 + H2O。n(NaOH)=2n(SO2)=0.2mol。V(NaOH)=n÷c=0.2mol÷4mol/L=0.05L.
CuSO4+SO2↑+2H2O,在反应方程式中,每产生1mol的SO2气体,电子转移2mol.。现在电子转移了0.2mol,所以产生了0.1mol的SO2气体。在标准状况下,其体积为2.24L。若用4 mol·L-1的NaOH溶液吸收生成的SO2,并生成正盐,则该反应的反应方程式为2NaOH + SO2 =Na2SO3 + H2O。n(NaOH)=2n(SO2)=0.2mol。V(NaOH)=n÷c=0.2mol÷4mol/L=0.05L.
考点:考查SO2气体的实验室制法、性质及有关反应的计算的知识。

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案金属铈(稀土元素)性质活泼。铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2。下列说法正确的是
| A.铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI = CeI4 + 2H2↑ |
| B.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4+ + Fe2+=Ce3+ + Fe3+ |
| C.在一定条件下,电解熔融状态的CeO2制Ce,在阳极获得铈 |
D.四种铈的核素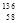 Ce、 Ce、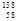 Ce、 Ce、 Ce、 Ce、 Ce,它们互称为同素异形体 Ce,它们互称为同素异形体 |
(15分)在航天发射时,肼(N2H4)及其衍生物常用作火箭推进剂。
⑴液态肼作火箭燃料时,与液态N2O4混合发生氧化还原反应,已知每1g肼充分反应后生成气态水放出热量为a KJ,试写出该反应的热化学方程式 。
⑵实验室用N2H4·H2O与NaOH颗粒一起蒸馏,收集114~116℃的馏分即为无水肼。
①在蒸馏过程中不需要的仪器是 (填序号字母)。
| A.酒精灯 | B.长直玻璃导管 | C.锥形瓶 | D.直型冷凝管 |
②除上述必需的仪器外,还缺少的主要玻璃仪器是 。
⑶肼能使锅炉内壁的铁锈变成较为致密的磁性氧化铁(Fe3O4)层,以减缓锅炉锈蚀。若反应过程中肼转化为氮气,则每生成1molFe3O4,需要消耗肼的质量为 g。
⑷磁性氧化铁(Fe3O4)的组成可写成FeO·Fe2O3。某化学实验小组通过实验来探究一黑色粉末是否由Fe3O4、CuO组成(不含有其它黑色物质)。探究过程如下:
提出假设:假设1. 黑色粉末是CuO;假设2. 黑色粉末是Fe3O4;
假设3. 。
探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
①若假设1成立,则实验现象是 。
②若所得溶液显血红色,则假设 成立。
③为进一步探究,继续向所得溶液加入足量铁粉,若产生 现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
④为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生 现象;若产生 现象,则假设3成立。
利用I2O5可消除CO污染或定量测定CO,反应为:5CO(g)+I2O5(s) 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1
(1)已知:2CO(g)+O2(g) 2CO2(g);ΔH 2
2CO2(g);ΔH 2
2I2(s)+5O2(g) 2I2O5(s);ΔH 3
2I2O5(s);ΔH 3
则ΔH 1= (用含ΔH 2和ΔH 3的代数式表示)。
(2)不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如图。请回答: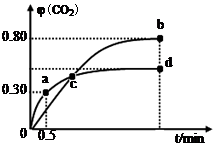
①从反应开始至a点时的反应速率为v(CO)= ,b点时化学平衡常数Kb= 。
②d点时,温度不变,若将容器体积压缩至原来的一半,请在图中补充画出CO2体积分数的变化曲线。
③下列说法正确的是 。(填字母序号)
| A.容器内气体密度不变,表明反应达到平衡状态 |
| B.两种温度下,c点时体系中混合气体的平均相对分子质量相等 |
| C.增加I2O5的投料量有利于提高CO的转化率 |
| D.b点和d点的化学平衡常数:Kb<Kd |
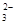 +I2===S4O
+I2===S4O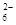 +2I-)
+2I-)

 →Fe(NO3)3+NO↑+2H2O
→Fe(NO3)3+NO↑+2H2O