题目内容
【题目】下列反应中,相关示意图错误的是
A | B | C | D |
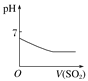
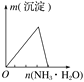
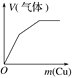
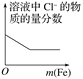
将二氧化硫通入到一定量氯水中 | 将氨水滴入到一定量氯化铝溶液中 | 将铜粉加入到一定量浓硝酸中 | 将铁粉加入到一定量氯化铁溶液中 |
|
|
|
|
A. A B. B C. C D. D
【答案】B
【解析】A、将二氧化硫通入到一定量氯水中,会发生反应:Cl2+SO2+2H2O=H2SO4+2HCl,最终是盐酸和硫酸,所以溶液的pH不变,选项A正确;B、将氨水滴入到一定量氯化铝溶液中,会发生反应:AlCl3+3NH3·H2O== Al(OH)3↓+3NH4Cl,Al(OH)3只能被强碱溶解,而NH3·H2O是弱碱,不能溶解,因此图像不符合,选项B错误;C、将铜粉加入到一定量浓硝酸中,首先发生反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,当反应进行到一定程度后溶液变稀,这时发生反应:3Cu+8HNO3(稀)=2Cu(NO3)2+2NO↑+4H2O,当硝酸反应完全后无论Cu还存在多少,都不再发生反应,因此符合题意,选项C正确;D、将铁粉加入到一定量氯化铁溶液中,2FeCl3+Fe==3FeCl2,Cl-的物质的量不变,但是由于溶液中Fe元素的质量增加,所以Cl元素的质量分数减少。当FeCl3完全反应后溶液的质量达到最大值,因此此时溶液中Cl元素的质量分数不变,选项D正确。答案选B。

【题目】一定条件下,CO2与NH3反应可制得重要的化工产品三聚氰胺:3NH3 + 3CO2![]()
 +3H2O。
+3H2O。
(1)基态N原子的价层电子排布图为____________,三聚氰胺的几种组成元素中电负性由大到小的顺序为____________(用元素符号表示)。
(2)三聚氰胺中氮原子的杂化轨道类型为____________。
(3)上述合成三聚氰胺的反应过程中存在多种类型化学键的断裂与形成,但这些化学键中不包括____________(填选项字母)。
a.α键 b.π键 c.非极性共价键 d.极性共价键
(4)三聚氰胺的熔点为250 ℃,则其晶体类型是____________,又知硝基苯的熔点为5.7 ℃,异致这两种物质熔点差异的原因是____________。
(5)随者科学技术的发展,科学家们已合成了由碳、氧两种元素形成的原子晶体.其晶胞结构如图(a) 所示:若晶胞参数为a pm,设NA表示阿伏加德罗常数的值,则该晶胞的密度是____________ g cm-3。
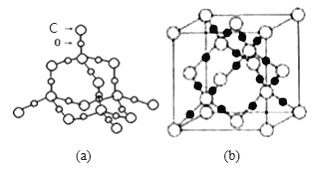
(6)SiO2晶体结构片断如图 (b)所示。通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
化学键 | Si-O | Si-Si | O=O |
键能/ KJ·mol-1 | 460 | 176 | 498 |
Si(s)+O2(g)![]() SiO2(s),该反应的反应热△H = ___________
SiO2(s),该反应的反应热△H = ___________
【题目】下表中对于相关物质的分类全部正确的是
选项 | 纯净物 | 混合物 | 非电解质 | 弱电解质 | 碱性氧化物 |
A. | 液氨 | 氢氧化铁胶体 | CO | 氢硫酸 | Al2O3 |
B. | 明矾 | 漂白粉 | 乙醇 | 硫酸钡 | Na2O |
C. | 碱石灰 | 碘酒 | Cl2 | HClO | K2O |
D. | 磁性氧化铁 | 水玻璃 | SO2 | 冰醋酸 | CaO |
A. A B. B C. C D. D