题目内容
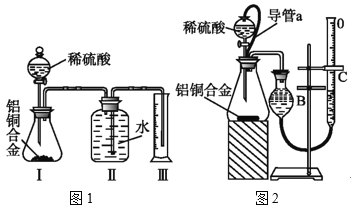
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解所得产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全,确定分解产物(铁的氧化物、硫的氧化物、含氮物质、水)的具体成分(已知每个装置中的药品足量)。
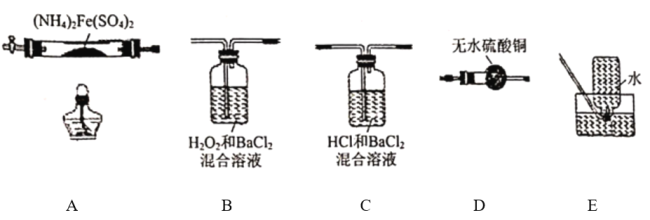
(1)利用上述装置完成该实验,则该装置的正确连接顺序为_______________(用装置下面的字母填连接顺序,每个装置都要使用)。加热A前需要通入一段时间N2目的是_______________。
(2)若观察到B中有白色沉淀生成,C中无明显现象,则装置C的作用为_______________,D中白色变为蓝色,写出B中发生反应的离子方程式_______________装置B与装置C能否互换_______________(填 “能”或“否”),原因是_______________(填“能”则不填此空)。
(3)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3,而不含FeO,请帮他完成表中内容(试剂,仪器和用品自选)。
实验步骤 | 预期现象 | 结论 |
_______________ | _______________ | 固本残留物仅为Fe2O3 |
(4)硫酸亚铁铵在500℃时隔绝空气加热完全分解,若E中收集到的气体只有N2,A中固体残留物Fe2O3的质量为80g,B中沉淀物质的量为2rnol,则生成N2的质量为_______________g。
(5)某含铬(Cr2O72-)废水用硫酸亚铁铵溶液滴定处理,反应后铁元素和铬元素完全转化为沉淀(沉淀中铬元素化合价为+3),该沉淀经干燥后得到amolFeOFemCrnO3,不考虑处理过程中的实际损耗,则消耗硫酸亚铁铵的物质的量为_______________mol(用a的代数式表示)。
【答案】ADCBE 实验前通入氮气是为了排除装置内的空气,防止对实验造成干扰,减少实验误差 检验生成的气体中是否有三氧化硫,并除去三氧化硫和氨气 SO2+H2O2+Ba2+=BaSO4↓+2H+ 否 若互换三氧化硫也会使B有白色沉淀生成,无法检验二氧化硫 取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解,将溶液分成两份,分别滴加高锰酸钾溶液、KSCN溶液; 若高锰酸溶液不褪色,加入KSCN溶液变红 14 2.5a
【解析】
硫酸亚铁铵受热分解产生的气体产物可能为二氧化硫、三氧化硫、水、氨气,A为硫酸亚铁铵受热分解的装置,有水产生时应先用无水硫酸铜检验水,D为检验水的装置,则A连D,氨气为碱性气体,极易溶于水,则氨气能溶于C装置中的溶液中,三氧化硫与水反应生成硫酸根,硫酸根与钡离子结合生成白色沉淀硫酸钡,由此可以检验并除去三氧化硫,C为检验三氧化硫并去除三氧化硫和氨气的装置,则D连C,二氧化硫在酸性溶液中溶解度极小,所以二氧化硫不溶于D,二氧化硫具有还原性,能被双氧水氧化成硫酸根而能与氯化钡生成硫酸钡白色沉淀,由此可以检验二氧化硫,B为检验二氧化硫的装置,则C连B,随后B连 E,由此可知,装置的正确连接顺序为ADCBE。
(1)由分析可知,装置的正确连接顺序为ADCBE,实验前通入氮气是为了排除装置内的空气,防止对实验造成干扰,减少实验误差,故答案为:ADCBE;实验前通入氮气是为了排除装置内的空气,防止对实验造成干扰,减少实验误差;
(2)由分析知,C为检验三氧化硫并去除三氧化硫和氨气的装置,除去三氧化硫是为了避免对二氧化硫的检验造成干扰;B中双氧水氧化二氧化硫并与氯化钡生成沉淀的离子方程式为SO2+H2O2+Ba2+=BaSO4↓+2H+;因为三氧化硫也能使B装置中产生白色沉淀,则无法检验产生的气体中是否含有二氧化硫,则装置B与装置C不能互换,故答案为:检验生成的气体中是否有三氧化硫,并除去三氧化硫和氨气;SO2+H2O2+Ba2+=BaSO4↓+2H+;否;若互换三氧化硫也会使B有白色沉淀生成,无法检验二氧化硫;
(3)验证固体残留物仅为Fe2O3,而不含FeO,则需将固体物质溶于酸,然后检验铁离子和亚铁离子即可,实验步骤为:取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解,将溶液分成两份,分别滴加高锰酸钾溶液、KSCN溶液;预期现象:若高锰酸溶液不褪色,加入KSCN溶液变红,故答案为:取少量A中残留物于试管中,加入适量稀硫酸,充分振荡使其完全溶解,将溶液分成两份,分别滴加高锰酸钾溶液、KSCN溶液;若高锰酸溶液不褪色,加入KSCN溶液变红;
(4)Fe2O3的质量为80g,物质的量为0.5mol,则硫酸亚铁铵的物质的量为1mol,硫原子的物质的量为2mol,而B装置中时二氧化硫最后转化成硫酸钡2mol,由此可知产物中无三氧化硫,则硫酸亚铁铵受热分解的方程式为2(NH4)2Fe(SO4)2![]() Fe2O3+2NH3↑+N2↑+4SO2↑+5H2O,m(N2)=
Fe2O3+2NH3↑+N2↑+4SO2↑+5H2O,m(N2)= ![]() =14g,故答案为:14;
=14g,故答案为:14;
(5)1mol亚铁离子被氧化后转化成铁离子,失去的电子为1mol,每生成1molCr3+转移的电子为3mol,根据元素得失电子守恒有3n=m,由根据FeOFemCrnO3中化合价的代数和为0,有3m+3n=6,解得m=1.5,n=0.5,则根据铁原子守恒,若得到amolFeOFemCrnO3需消耗硫酸亚铁铵的物质的量为(1+m)a=(1+1.5)a=2.5amol,故答案为:2.5a。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案【题目】氯气有毒,且大量制取的难度较大、污染严重,在培养皿中研究氯气的性质可实现“绿色实验”。在培养皿的点滴板中央孔穴中滴加能生成氯气的试剂(如漂白精与盐酸),然后分别滴加所要进行实验的试剂,如图。下列是某学生观察到的现象、解释与结论,其中不符合事实的是

选项 | 实验现象 | 解释 | 结论 |
A | 淀粉KI溶液变蓝 | 氯气置换出KI中的碘使淀粉变蓝 | 单质氧化性:Cl2>I2 |
B | Na2S溶液中出现淡黄色沉淀 | 氯气置换出Na2S中的硫 | 单质氧化性:Cl2>S |
C | 湿润的蓝色石蕊试纸先变红后褪色 | 氯气与水反应生成盐酸和次氯酸 | 氯气具有漂白性 |
D | FeCl2和KSCN溶液的小液滴变红 | FeCl2被Cl2氧化成FeCl3后,再与KSCN溶液反应变红 | 氯气具有氧化性 |
A.AB.BC.CD.D