题目内容
【题目】科学家对一碳化学进行了广泛深入的研究并取得了一些重要成果。
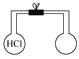
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气。下图表示恒压容器中0.5molCO2和1.5molH2转化率达80%时的能量变化示意图。写出该反应的热化学方程式:__________________。

(2)现向三个体积均为2L的恒容密闭容器Ⅰ、Ⅱ、Ⅲ中均分别充入lmolCO和2molH2发生反应:CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.1kJ/mol。三个容器的反应温度分别为T1、T2、T3且恒定不变,当反应均进行到5min时H2的体积分数如图所示,其中只有一个容器中的反应己经达到平衡状态.
CH3OH(g) △H1=-90.1kJ/mol。三个容器的反应温度分别为T1、T2、T3且恒定不变,当反应均进行到5min时H2的体积分数如图所示,其中只有一个容器中的反应己经达到平衡状态.

① 三个容器中一定达到平衡状态的是容器_____(填序号,下同)
②0~5min时间内容器I中用CH3OH表示的化学反应速率为__________。
③ 当三个容器中的反应均达到平衡状态时CO 的转化率最高的是容器_____;平衡常数最小的是容器______。
(3)CO常用于工业冶炼金属.右下图是在不同温度下CO还原四种金属氧化物达平衡后气体中lg[![]() ]与温度(t)的关系曲线图。下列说法正确的是_______。
]与温度(t)的关系曲线图。下列说法正确的是_______。

A.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属铬(Cr)
C.工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率
D.CO还原PbO2的反应△H>O
(4)某工厂工业废水中含有甲醛,该厂降解甲醛的反应机理如图所示,则X表示的粒子是____,总反应的化学方程式为_________。

【答案】 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49kJ/mol Ⅲ 0.067 mol/(L·min) I Ⅲ BC( HCO3- ,HCHO+O2
CH3OH(g)+H2O(g) △H=-49kJ/mol Ⅲ 0.067 mol/(L·min) I Ⅲ BC( HCO3- ,HCHO+O2![]() CO2+H2O
CO2+H2O
【解析】(1)由恒压容器中0.5molCO2和1.5molH2转化率达80%时的能量变化示意图可知,0.5molCO2和1.5molH2转化率达80%时的能量变化为3.4kJ/mol-23kJ/mol=19.6kJ/mol,由此求出1molCO2和3molH2转化率达100%时的能量变化为49kJ/mol,所以该反应的热化学方程式为CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49kJ/mol。
CH3OH(g)+H2O(g) △H=-49kJ/mol。
(2)由图像可知,T3>T2>T1,所以反应前5min的平均速率为III>II>I,从速率方面讲,最先到达平衡状态的一定是III,由于该反应△H1<0为放热反应,该反应的化学平衡常数随温度升高而减小,所以从反应限度方面讲,最先到达平衡状态的也一定是III。
① 三个容器中一定达到平衡状态的是容器III。
②设0~5min时间内容器I中CO(g)+2H2(g)![]() CH3OH(g)氢气的转化率为x
CH3OH(g)氢气的转化率为x
起始量(mol) 1 2 0
变化量(mol) x 2![]() x
x
5min量(mol) 1- x 2-2x x
由氢气的体积分数为0.4=![]() ,解之得x=0.67,则用CH3OH表示的化学反应速率为
,解之得x=0.67,则用CH3OH表示的化学反应速率为![]() =0.067 mol/(L·min) 。
=0.067 mol/(L·min) 。
③ 当三个容器中的反应均达到平衡状态时,KI>KII>KIII,CO 的转化率最高的是容器I;平衡常数最小的是容器III。
(3)在平衡体系中,lg[![]() ]的值越小,说明反应的CO的转化率越高,金属氧化物越容易被还原,反之则越低,金属氧化物越难被还原。由达平衡后气体中lg[
]的值越小,说明反应的CO的转化率越高,金属氧化物越容易被还原,反之则越低,金属氧化物越难被还原。由达平衡后气体中lg[![]() ]与温度(t)的关系曲线图可知:A.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量,这个说法不正确,在平衡状态下,CO的百分含量是保持不变的;B.由图可知,即使在1300℃,lg[
]与温度(t)的关系曲线图可知:A.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量,这个说法不正确,在平衡状态下,CO的百分含量是保持不变的;B.由图可知,即使在1300℃,lg[![]() ]>2,
]>2, ![]() >102,则Cr2O3(s)+3CO(g)
>102,则Cr2O3(s)+3CO(g)![]() 2Cr(s)+3CO2(g),K=
2Cr(s)+3CO2(g),K=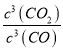 <10-6,所以CO不适宜用于工业冶炼金属铬(Cr)是正确的;C.由图可知,在较低的温度下,lg[
<10-6,所以CO不适宜用于工业冶炼金属铬(Cr)是正确的;C.由图可知,在较低的温度下,lg[![]() ]的值较小,所以工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率是正确的;D.由图像可知,CO还原PbO2的反应中lg[
]的值较小,所以工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率是正确的;D.由图像可知,CO还原PbO2的反应中lg[![]() ]的值随温度升高而增大,说明该反应的化学平衡常数随温度升高而减小,所以该反应为放热反应,△H<O ,D不正确。综上所述BC正确。
]的值随温度升高而增大,说明该反应的化学平衡常数随温度升高而减小,所以该反应为放热反应,△H<O ,D不正确。综上所述BC正确。
(4)由图可知,-CHO与O2-反应后生成X,而X与H+反应生成的是CO2,所以X表示的粒子是HCO3-,总反应的化学方程式为,HCHO+O2![]() CO2+H2O。
CO2+H2O。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】丙烯酸的结构简式为CH2=CH—COOH,对其性质的描述不正确的是( )
A.能与金属钠反应放出氢气B.能与新制氢氧化铜反应
C.能发生加聚反应生成高分子化合物D.能与溴水发生取代反应而使溴水褪色
【题目】五种短周期元素的部分性质数据如下:
元素 | T | X | Y | Z | W |
原子半径(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
最高或最低化合价 | +1 | +5,-3 | +7,-1 | +6,-2 | +3 |
请回答下列问题:
(1)Z离子的结构示意图为________________。
(2)关于Y、Z两种元素,下列叙述正确的是________(填序号)
a.简单离子的半径Y>Z
b.气态氢化物的稳定性Y比Z强
c.最高价氧化物对应水化物的酸性Z比Y强
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物。
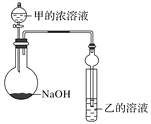
某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中立即有甲放出,原因是______________________。
一段时间后,观察到试管中的现象是______________________________,发生反应的离子方程式是______________________________________________。
(4)XO2是导致光化学烟雾的“罪魁祸首”之一。它被NaOH溶液吸收的化学方程式是:2XO2+2NaOH===M+NaXO3+H2O(已配平),产物M中元素X的化合价为____________________。