题目内容
【题目】硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量Fe2O3 、FeCO3 、MgO、CaO等,生产工艺流程图如下:
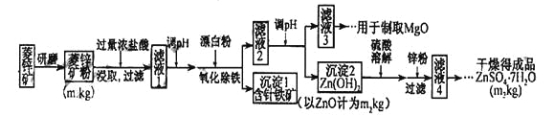
(1)将菱锌矿研磨成粉的目的是___________________。
(2)完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)2+ □____+ □_____="=" □Fe(OH)3+ □Cl_
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H ,化学式式量为89,化学式是_______ 。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为______ 。
Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
开始沉淀的pH | 10.4 | 6.4 | — | — |
沉淀完全的pH | 12.4 | 8.0 | — | — |
开始溶解的pH | — | 10.5 | — | — |
Ksp | 5.6×10-12 | — | 6.8×10-6 | 2.8×10-9 |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是_________(选填序号)。
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为 ______ 、_______ 、过滤,洗涤,干燥。
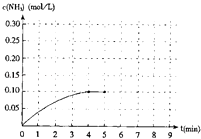
(7)分析图中数据,菱锌矿粉中ZnC3的质量分数不低于 。
【答案】(1) 增大接触面积,加快反应速率,使反应更充分
(2)2Fe(OH)2+ 1 ClO+ 1H2O ="=" 2Fe(OH)3+ 1Cl_
((3)FeO(OH) (4) 8.0≤pH<10.4 (5) bd
(6) 蒸发浓缩 、 冷却结晶 (7) (125m2/81m1)×100%
【解析】试题分析:(1)将菱锌矿研磨成粉可以增加反应时的接触面积,使得反应更加充分。
(2)流程中“氧化除铁”是加入漂白粉,方程式后面产物中又有氯离子,可知氧化剂是ClO-,观察方程式前后可以推出还要加入水分子,据原子守恒配平得:2Fe(OH)2+ 1 ClO+ 1H2O ="=" 2Fe(OH)3+ 1Cl_。
(3)化学式量为89,组成元素是Fe、O、H,其中铁的相对原子量为56,扣掉56剩下33,化学式中只能含有2个氧原子和1个氢原子,所以可能的组成为FeO(OH)。
(4)调节滤液2的PH要想生成Zn(OH)2沉淀而不生成Mg(OH)2,必须知道Mg(OH)2开始沉淀时的pH、Zn(OH)2开始沉淀时的pH,Mg(OH)2沉淀完全时的pH、Zn(OH)2沉淀完全时的pH,pH应介于8.0≤pH<10.4。
(5)从“滤液3”制取MgO过程中,应先生成Mg(OH)2,溶液碱性应较强,bd符合,而纯碱溶液水解呈碱性,碱性较弱。
(6)“滤液4”之后的操作目的是得到纯净的固体,应将溶液蒸发、结晶、过滤后洗涤并干燥。
(7)设碳酸锌的质量为m,利用关系式法计算:ZnCO3----ZnO
125 81
m m2
ZnCO3的质量为125m2/81,ZnCO3的质量分数为 125m2/81m1。

【题目】如表是食用碘盐包装上的部分说明,下列说法正确的是( )
配料 | 精盐、碘酸钾、抗结剂 |
碘含量 | 35±15mgkg﹣1 |
储存方法 | 密封、避光、防潮 |
食用方法 | 烹饪时,待食品熟后加入碘盐 |
A.高温会导致碘的损失
B.碘酸钾可氧化氯化钠
C.可用淀粉检验碘盐中的碘酸钾
D.该碘盐中碘酸钾含量为20~50 mgkg﹣1