题目内容
【化学—化学与技术】(12分)硫酸工业流程如下所示:
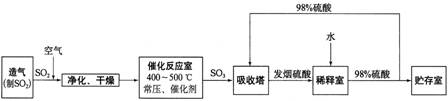
(1)催化反应室发生反应的化学方程式是: 。该反应通常用 V2O5 作催化剂,其催化机理可能是:V2O5 氧化 SO2 时,自身被还原为四价钒化合物;四价钒化合物再被 O2 氧化。写出该催化循环机理的化学方程式:
。
(2)依据流程图判断下列说法正确的是 (填字母)。
a.过量空气能提高 SO2 的转化率
b.使用催化剂能提高 SO2 的反应速率和转化率
c.用 98%的硫酸吸收 SO3 ,可以避免形成酸雾并提高吸收率
(3)每160g SO3 气体与 H2O (l) 化合放出 260.6 kJ 的热量,该反应的热化学方程式是 。
(4)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理。这样做除了防止SO2 污染环境并得到铵盐外,主要目的是: 。
【答案】
(1)2SO2 (g) +
O2 (g)  2SO3 (g)(2分)。
2SO3 (g)(2分)。
SO2 +V2O5 = SO3 +2VO2(2分); O2 + 4VO2 = 2V2O5(2分);
(2) a、c(2分)。
(3)SO3 (g) + H2O (l) = H2SO4 (l) ;△H=-130.3 kJ/mol(2分)。
(4)得到较高浓度的SO2 ,原料循环再利用(2分)。
【解析】

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目



