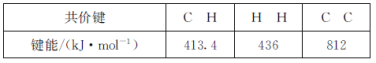
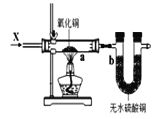
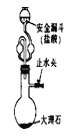
题目内容
【题目】短周期元素X、Y、Z、W的原子序数依次增大.X原子核内没有中子;Z与W在周期表中同主族,且Y、Z和W三种元素的原子最外层电子数之和为17;X、Y形成的化合物M的水溶液呈碱性.则下列说法不正确的是![]()
A.原子半径:![]()
B.标准状况下的![]() LM溶于水,所得溶液
LM溶于水,所得溶液![]()
C.![]() 能使湿润的淀粉KI试纸变蓝
能使湿润的淀粉KI试纸变蓝
D.一定条件下,Cu可与W的最高价氧化物对应水化物发生反应
【答案】B
【解析】
短周期元素X、Y、Z、W的原子序数依次增大,X原子核内没有中子,则X为H元素;X、Y形成的化合物M的水溶液呈碱性,则Y是N元素,M为![]() ;
;
Z与W在周期表中同主族,且Y、Z和W三种元素的原子最外层电子数之和为17,则Z和W最外层电子数都是6,且Z原子序数小于W,所以Z是O、W是S元素。
A.原子电子层数越多其原子半径越大,同一周期元素,原子半径随着原子序数增大而减小,所以原子半径:![]() ,故A不符合题意;
,故A不符合题意;
B.标况下![]() 氨气的物质的量是
氨气的物质的量是![]() ,
,![]() 氨气溶于水得到氨水,溶液的体积未知导致无法计算氨水物质的量浓度,且一水合氨是弱电解质,部分电离,所以无法计算溶液的pH,故B符合题意;
氨气溶于水得到氨水,溶液的体积未知导致无法计算氨水物质的量浓度,且一水合氨是弱电解质,部分电离,所以无法计算溶液的pH,故B符合题意;
C.![]() 具有氧化性,能氧化碘离子生成碘单质,碘遇淀粉试液变蓝色,所以
具有氧化性,能氧化碘离子生成碘单质,碘遇淀粉试液变蓝色,所以![]() 能使湿润的淀粉KI试纸变蓝,故C不符合题意;
能使湿润的淀粉KI试纸变蓝,故C不符合题意;
D.W是S元素,其最高价氧化物的水化物是硫酸,加热条件下,Cu能和浓硫酸反应生成硫酸铜、二氧化硫和水,故D不符合题意;
故选:B。

 阅读快车系列答案
阅读快车系列答案【题目】有一无色透明溶液,欲确定是否含有下列离子:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,取该溶液的实验如下:
,取该溶液的实验如下:
实验步骤 | 实验现象 |
| 溶液变红色 |
| 有无色气体产生,气体遇空气可以变成红棕色 |
| 有白色沉淀生成 |
| 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
由此判断,下列说法正确的是![]()
A.根据实验![]() 可以确定溶液中不含有
可以确定溶液中不含有![]() 和
和![]() ,因为这二个离子相对应的酸为弱酸
,因为这二个离子相对应的酸为弱酸
B.溶液中一定存在的离子是![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ;溶液中肯定不存在的离子是:
;溶液中肯定不存在的离子是:![]() 、
、![]() 、
、![]() 、
、![]()
C.为进一步确定其它离子,应该补充焰色反应的实验来检验![]() 就可以
就可以
D.通过实验![]() 和
和![]() 就可以确定溶液中一定含有
就可以确定溶液中一定含有![]() ,一定不含有
,一定不含有![]() 、
、![]() 、
、![]() ,所以实验步骤
,所以实验步骤![]() 的设计是错误的
的设计是错误的