题目内容
(7分)将1 mol CO和1 mol H2O充入某固定容积的容器中,在某条件下达到平衡:CO(g)+H2O(g) CO2(g)+H2(g),此时有
CO2(g)+H2(g),此时有 的CO转化为CO2。计算平衡状态下混合气体中CO2的体积分数。
的CO转化为CO2。计算平衡状态下混合气体中CO2的体积分数。
 CO2(g)+H2(g),此时有
CO2(g)+H2(g),此时有 的CO转化为CO2。计算平衡状态下混合气体中CO2的体积分数。
的CO转化为CO2。计算平衡状态下混合气体中CO2的体积分数。33.3%
由于该反应是气体分子数目不变的反应,所以最后混合气体共有2 mol,而生成的CO2是 mol,所以平衡时CO2的体积分数为:
mol,所以平衡时CO2的体积分数为: mol×
mol×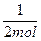 ×100%=33.3%。
×100%=33.3%。
 mol,所以平衡时CO2的体积分数为:
mol,所以平衡时CO2的体积分数为: mol×
mol×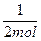 ×100%=33.3%。
×100%=33.3%。
练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
 2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。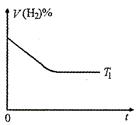 (2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
(2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。 2CO(g)(吸热反应)
2CO(g)(吸热反应) 2Z(g),已知X2、Y2、Z的起始量分别为0.10 mol、0.3 mol、 0.2 mol,一定条件下达到平衡时,各组分的物质的量有可能是( )
2Z(g),已知X2、Y2、Z的起始量分别为0.10 mol、0.3 mol、 0.2 mol,一定条件下达到平衡时,各组分的物质的量有可能是( ) Na2S(s)+4H2O(g);ΔH>0
Na2S(s)+4H2O(g);ΔH>0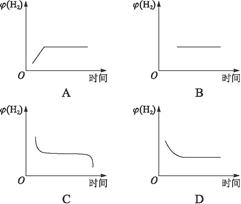
 2SO3(气)
2SO3(气) cC(g)+dD(g),达平衡后,改变某条件时,发生右图所示的变化,下列选项叙述正确的是( )
cC(g)+dD(g),达平衡后,改变某条件时,发生右图所示的变化,下列选项叙述正确的是( )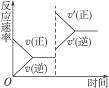
 2C(g) ,甲恒容、乙恒压,温度相同而恒定。起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02molC,开始时两容器压强相等,最后分别达到平衡。下列有关它们平衡状态的叙述正确的是( )
2C(g) ,甲恒容、乙恒压,温度相同而恒定。起始时甲中加入0.01mol A和0.03mol B,乙中加入0.02molC,开始时两容器压强相等,最后分别达到平衡。下列有关它们平衡状态的叙述正确的是( )