题目内容
已知A~K所代表的各物质都是中学化学里常见的物质,且I是具有磁性的物质,D和K都具有两性.一定条件下,各物质间的相互反应转化关系如图所示:
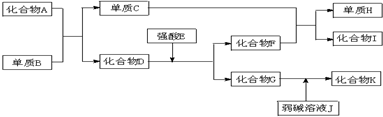
请回答:
(1)写出有关物质化学式:D是 ,K是 ,H是 .
(2)写出下列反应的方程式:
①化合物G的溶液不呈中性,其原因用离子方程式表示为 ;
②C+F→H+I .

请回答:
(1)写出有关物质化学式:D是
(2)写出下列反应的方程式:
①化合物G的溶液不呈中性,其原因用离子方程式表示为
②C+F→H+I
考点:无机物的推断
专题:推断题
分析:I是具有磁性的物质,应为Fe3O4,单质C与化合物F反应得到单质H与化合物I,由元素守恒可知C为Fe,D和K都具有两性,分别为氧化铝、氢氧化铝中的一种,单质B与化合物A反应得到Fe与D,该反应为铝热反应,可推知B为Al、A为Fe2O3、D为Al2O3,顺推可知F为H2O,G为AlCl3,H为H2,弱碱溶液J为氨水,K为Al(OH)3,据此解答.
解答:
解:I是具有磁性的物质,应为Fe3O4,单质C与化合物F反应得到单质H与化合物I,由元素守恒可知C为Fe,D和K都具有两性,分别为氧化铝、氢氧化铝中的一种,单质B与化合物A反应得到Fe与D,该反应为铝热反应,可推知B为Al、A为Fe2O3、D为Al2O3,顺推可知F为H2O,G为AlCl3,H为H2,弱碱溶液J为氨水,K为Al(OH)3,
(1)由上述分析可知,D是Al2O3,K是Al(OH)3,H是H2,故答案为:Al2O3;Al(OH)3;H2;
(2)①AlCl3溶液中铝离子水解:Al3++3H2O?Al(OH)3+3H+,破坏水的电离平衡,溶液呈酸性,故答案为:Al3++3H2O?Al(OH)3+3H+;
②C+F→H+I的反应方程式为:3Fe+4H2O(g)
Fe3O4+4H2,故答案为:3Fe+4H2O(g)
Fe3O4+4H2.
(1)由上述分析可知,D是Al2O3,K是Al(OH)3,H是H2,故答案为:Al2O3;Al(OH)3;H2;
(2)①AlCl3溶液中铝离子水解:Al3++3H2O?Al(OH)3+3H+,破坏水的电离平衡,溶液呈酸性,故答案为:Al3++3H2O?Al(OH)3+3H+;
②C+F→H+I的反应方程式为:3Fe+4H2O(g)
| ||
| ||
点评:本题考查无机物推断,涉及Fe、Al元素化合物性质,“I是具有磁性的物质,D和K都具有两性”是推断突破口,再结合转化关系推断,需要学生熟练掌握元素化合物知识,难度中等.

练习册系列答案
相关题目
下列铵盐的叙述正确的是( )①铵盐易溶于水②铵盐中的氮元素均为-3价③铵盐受热易分解④铵盐都能与碱反应⑤铵盐都不能与酸反应.
| A、①②③ | B、①③④ |
| C、②③④ | D、全部 |
同温同压下,相同物质的量的CO和N2,具有相同的( )
| A、原子数 | B、质子数 |
| C、体积 | D、质量 |