题目内容
(7分)按要求填空:
(1)某阴离子核外18电子,带两个单位负电荷,其离子结构示意图 。
(2)含6个质子、8个中子的原子符号为 ,它与16O形成3原子分子甲,4.6克甲的物质的量是 mol,甲分子中相邻原子间以 键结合(填“离子键”或“共价键”)。
(3)铁原子核外有4个电子层,在周期表第8列,它在元素周期表的第 周期 族。
(4)盛放碱液的试剂瓶不能用玻璃塞,是为了防止发生
反应(以NaOH为例用化学方程式表示),避免瓶塞与瓶口粘在一起
(1)某阴离子核外18电子,带两个单位负电荷,其离子结构示意图 。
(2)含6个质子、8个中子的原子符号为 ,它与16O形成3原子分子甲,4.6克甲的物质的量是 mol,甲分子中相邻原子间以 键结合(填“离子键”或“共价键”)。
(3)铁原子核外有4个电子层,在周期表第8列,它在元素周期表的第 周期 族。
(4)盛放碱液的试剂瓶不能用玻璃塞,是为了防止发生
反应(以NaOH为例用化学方程式表示),避免瓶塞与瓶口粘在一起
(1) S2- 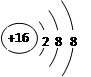 (2)(1+1+1分) 146C, 0.1,共价键
(2)(1+1+1分) 146C, 0.1,共价键
(3)(1分)四,第Ⅷ
(4)(2分)SiO2 + 2NaOH = Na2 CO3+ H2O
 (2)(1+1+1分) 146C, 0.1,共价键
(2)(1+1+1分) 146C, 0.1,共价键 (3)(1分)四,第Ⅷ
(4)(2分)SiO2 + 2NaOH = Na2 CO3+ H2O
(1)离子结构示意图为

(2)含6个质子、8个中子的原子符号为146C,甲的物质的量0.1mol,甲分子中相邻原子间以共价键结合
(3)铁在元素周期表的第四周期第Ⅷ族
(4)为了防止发生SiO2 + 2NaOH = Na2 CO3+ H2O

(2)含6个质子、8个中子的原子符号为146C,甲的物质的量0.1mol,甲分子中相邻原子间以共价键结合
(3)铁在元素周期表的第四周期第Ⅷ族
(4)为了防止发生SiO2 + 2NaOH = Na2 CO3+ H2O

练习册系列答案
相关题目
 X
X