题目内容
已知: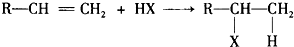
A、B、C、D、E有如图所示转化关系:
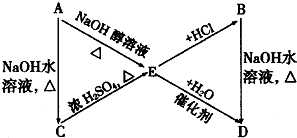
其中A、B分别是化学式为C3H7Cl的两种同分异构体.根据图中各物质的转化关系,填写下列空白:
(1)A、B、C、D、E的结构简式:A
 、C
、C
 、E
、E
(2)完成下列反应的化学方程式:①A→E +NaOH
+NaOH
 +NaCl
+NaCl +NaOH
+NaOH
 +NaCl;③C→E
+NaCl;③C→E
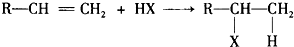
A、B、C、D、E有如图所示转化关系:

其中A、B分别是化学式为C3H7Cl的两种同分异构体.根据图中各物质的转化关系,填写下列空白:
(1)A、B、C、D、E的结构简式:A
CH3CH2CH2Cl
CH3CH2CH2Cl
、B

CH3CH2CH2OH
CH3CH2CH2OH
、D

CH3CH=CH2
CH3CH=CH2
.(2)完成下列反应的化学方程式:①A→E
CH3CH2CH2Cl+NaOH
CH3CH=CH2↑+NaCl+H2O
| 乙醇 |
| △ |
CH3CH2CH2Cl+NaOH
CH3CH=CH2↑+NaCl+H2O
;②B→D| 乙醇 |
| △ |
 +NaOH
+NaOH| 水 |
| △ |
 +NaCl
+NaCl +NaOH
+NaOH| 水 |
| △ |
 +NaCl
+NaClCH3CH2CH2OH
CH3CH=CH2+H2O
| 浓硫酸 |
| △ |
CH3CH2CH2OH
CH3CH=CH2+H2O
.| 浓硫酸 |
| △ |
分析:C3H7Cl的两种同分异构体分别为CH3CH2CH2Cl和 ,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为
,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为 ,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为
,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为 ,结合有机物的结构和性质以及题目要求可解答该题.
,结合有机物的结构和性质以及题目要求可解答该题.
 ,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为
,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为 ,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为
,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为 ,结合有机物的结构和性质以及题目要求可解答该题.
,结合有机物的结构和性质以及题目要求可解答该题.解答:解:C3H7Cl的两种同分异构体分别为CH3CH2CH2Cl和 ,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为
,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为 ,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为
,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为 ,
,
(1)由以上分析可知A为CH3CH2CH2Cl,B为 ,C为CH3CH2CH2OH,D为
,C为CH3CH2CH2OH,D为 ,E为CH3CH=CH2,
,E为CH3CH=CH2,
故答案为:CH3CH2CH2Cl; ;CH3CH2CH2OH;
;CH3CH2CH2OH; ;CH3CH=CH2;
;CH3CH=CH2;
(2)A为CH3CH2CH2Cl,可在NaOH醇溶液中发生消去反应生成CH3CH=CH2,反应的化学方程式为CH3CH2CH2Cl+NaOH
CH3CH=CH2↑+NaCl+H2O,
B为 ,可在碱性条件下发生水解,反应的方程式为
,可在碱性条件下发生水解,反应的方程式为 +NaOH
+NaOH
 +NaCl,
+NaCl,
C为CH3CH2CH2OH,可在浓硫酸作用下加热发生消去反应生成CH3CH=CH2,反应的方程式为CH3CH2CH2OH
CH3CH=CH2+H2O,
故答案为:CH3CH2CH2Cl+NaOH
CH3CH=CH2↑+NaCl+H2O; +NaOH
+NaOH
 +NaCl;CH3CH2CH2OH
+NaCl;CH3CH2CH2OH
CH3CH=CH2+H2O.
 ,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为
,A不论是二者中的哪一种结构,当在NaOH醇溶液中发生反应时只生成一种结构:CH3CH=CH2,即E为CH3CH=CH2,根据题目所给信息可知B为 ,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为
,则A为CH3CH2CH2Cl,进一步可知C为CH3CH2CH2OH,D为 ,
,(1)由以上分析可知A为CH3CH2CH2Cl,B为
 ,C为CH3CH2CH2OH,D为
,C为CH3CH2CH2OH,D为 ,E为CH3CH=CH2,
,E为CH3CH=CH2,故答案为:CH3CH2CH2Cl;
 ;CH3CH2CH2OH;
;CH3CH2CH2OH; ;CH3CH=CH2;
;CH3CH=CH2;(2)A为CH3CH2CH2Cl,可在NaOH醇溶液中发生消去反应生成CH3CH=CH2,反应的化学方程式为CH3CH2CH2Cl+NaOH
| 乙醇 |
| △ |
B为
 ,可在碱性条件下发生水解,反应的方程式为
,可在碱性条件下发生水解,反应的方程式为 +NaOH
+NaOH| 水 |
| △ |
 +NaCl,
+NaCl,C为CH3CH2CH2OH,可在浓硫酸作用下加热发生消去反应生成CH3CH=CH2,反应的方程式为CH3CH2CH2OH
| 浓硫酸 |
| △ |
故答案为:CH3CH2CH2Cl+NaOH
| 乙醇 |
| △ |
 +NaOH
+NaOH| 水 |
| △ |
 +NaCl;CH3CH2CH2OH
+NaCl;CH3CH2CH2OH| 浓硫酸 |
| △ |
点评:本题考查有机物的推断,题目难度不大,本题注意以E为突破口结合题目信息推断,明确同分异构体的判断为解答该题的关键,注意把握有机物的官能团的结构和性质.

练习册系列答案
相关题目
 (2011?新余二模)化学--选修物质结构与性质
(2011?新余二模)化学--选修物质结构与性质
 已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
已知:A、B、C、D、E、F、X为周期表中前四周期的七种元素,它们的原子序数依次增大.A是周期表中原子半径最小的元素;B的基态原子有3个不同的能级,各能级中电子数相等;D的基态原子2p能级上的未成对电子数与B原子的相同;D2-离子与E2+离子具有相同的稳定电子层结构;F有“生物金属”之称,F4+离子和氩原子的核外电子排布相同;X的基态原子的价电子排布式为3d84s2.
 已知单质A、B、C、D有如下的反应关系.其中A 在B中燃烧时,火焰呈苍白色; C在B中燃烧时生成棕黄色的烟,E的水溶液呈蓝绿色,G是一种黑色固体.
已知单质A、B、C、D有如下的反应关系.其中A 在B中燃烧时,火焰呈苍白色; C在B中燃烧时生成棕黄色的烟,E的水溶液呈蓝绿色,G是一种黑色固体.