题目内容
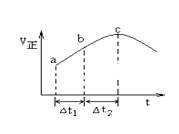
【题目】某pH =1的溶液X,其中可能含有Al3+、Fe2+、Fe3+、Ba2+、NH4+、CO32-、SO42-、SiO32-、NO3-中的一种或几种,取500 mL该溶液进行实验,其现象及转化如图所示。
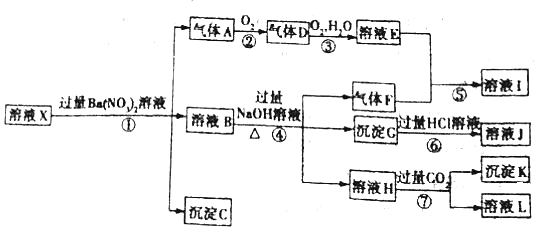
已知:反应过程中有一种气体是红棕色。请回答下列问题:
(1)仅由强酸性条件便可判断溶液X中一定不存在的离子有______。
(2)溶液X中,关于NO3-的判断一定正确的是______![]() 填字母
填字母![]() 。
。
a.一定有
b.一定没有
c.可能有
(3)反应①中产生气体A的离子方程式为______。
(4)反应⑦中生成沉淀K的离子方程式为______。
(5)溶液X中不能确定的离子是______。
(6)若实验测定A、F、K均为0.01 mol,试确定沉淀C是______,其物质的量范围是______。
【答案】CO32-、SiO32- b 3Fe2+ + NO3- + 4H+ = 3Fe3+ + NO↑ + 2H2O CO2 + AlO2- + 2H2O = Al(OH)3↓ + HCO3- Fe3+ BaSO4 ≥0.075 mol
【解析】
某强酸性溶液X,则溶液中不存在弱酸根离子CO32-、SiO32-,溶液和硝酸钡溶液反应生成沉淀C,则溶液呈存在SO42-,不存在和硫酸根离子反应的Ba2+,C是BaSO4;酸性条件下硝酸根离子具有强氧化性,所以溶液中Fe2+和NO3-不能共存,加入硝酸钡产生气体,则溶液中存在Fe2+,不存在NO3-,A是NO;溶液B中加入氢氧化钠溶液时,产生气体F,则溶液中含有NH4+,F是NH3,产生沉淀,则溶液中存在Fe3+,沉淀G是Fe(OH)3,氢氧化铁和盐酸反应生成FeCl3,则J是FeCl3,溶液H中通入过量二氧化碳生成沉淀,则溶液中存在Al3+,沉淀K是Al(OH)3,溶液L是NaHCO3;A是NO,则D是NO2,二氧化氮化和水反应生成硝酸和NO,则E是HNO3,硝酸和氨气反应生成硝酸铵,则I是NH4NO3,以此解答该题。
⑴由强酸性条件即可判断溶液X中一定不存在弱酸根离子,所以不存在的离子有CO32-、SiO32-,故答案为:CO32-、SiO32-。
⑵强酸性溶液中硝酸根离子具有强氧化性,如果存在硝酸根离子,则不存在亚铁离子,加入硝酸钡溶液时不能产生气体,所以溶液X中一定没有NO3-,故答案为:b。
⑶亚铁离子和硝酸反应生成铁离子、一氧化氮和水,离子反应方程式为:
3Fe2+ + NO3- + 4H+ = 3Fe3+ + NO↑ + 2H2O,故答案为:3Fe2+ + NO3- + 4H+ = 3Fe3+ + NO↑ + 2H2O。
⑷⑦中生成沉淀K的离子方程式为CO2 + AlO2- + 2H2O = Al(OH)3↓ + HCO3-,故答案为:CO2 + AlO2- + 2H2O = Al(OH)3↓ + HCO3-。
⑸溶液中存在Fe2+,可被氧化生成Fe3+,则不能确定原溶液是否含有Fe3+;故答案为:Fe3+。
![]() 、F、K均为0.01 mol,500 mL X溶液中n(H+)=0.05mol,根据反应3Fe2+ + NO3- + 4H+ = 3Fe3+ + NO↑ + 2H2O,可知亚铁离子为0.03mol,根据溶液电中性可知:
、F、K均为0.01 mol,500 mL X溶液中n(H+)=0.05mol,根据反应3Fe2+ + NO3- + 4H+ = 3Fe3+ + NO↑ + 2H2O,可知亚铁离子为0.03mol,根据溶液电中性可知:
3n(Al3+)+2 n(Fe2+) + n(NH4+) + n(H+) = 2n(SO42-),n(SO42-) =![]() ,当X溶液中不能确定的离子是Fe3+,则硫酸根离子的物质的量大于0.075 mol,生成沉淀C硫酸钡的物质的量大于0.075 mol;故答案为:BaSO4;≥0.075 mol。
,当X溶液中不能确定的离子是Fe3+,则硫酸根离子的物质的量大于0.075 mol,生成沉淀C硫酸钡的物质的量大于0.075 mol;故答案为:BaSO4;≥0.075 mol。

【题目】为测定碱式碳酸钴[COx(OH)y(CO3)z]的化学组成,研究性学习小组的同学设计了如图所示的装置进行实验探究。已知:碱式碳酸钴受热时可分解生成三种氧化物。
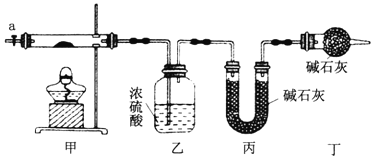
(1)按如图所示装置组装好仪器,并___________;称取3.65g样品置于硬质玻璃管内,加热,当乙装置中_______(填实验现象),停止加热;打开活塞a,缓缓通入空气数分钟,通入空气的目的是__________。
(2)某同学认为上述实验中存在一个缺陷,该缺陷是_________。
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为__________。
(4)CoCl2·6H2O常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取COCl2·6H2O的一种工艺如下:
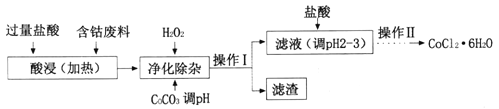
已知:25℃时
沉淀物 | Fe(OH)3 | Fe(OH)2 | CO(OH)2 | Al(OH)3 |
开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
①净化除杂时,加入H2O2发生反应的离子方程式为______________;
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为_________;
③加盐酸调整pH为2~3的目的为___________;
④操作Ⅱ过程为蒸发浓缩、冷却结晶、过滤。