题目内容
【题目】今有铁、水、氧化钙、碳酸钙、氢氧化钠溶液、硫酸铜溶液等六种物质,从中选出适当的物质按下述要求写出一个化学方程式。
(1)化合反应________________________
(2)分解反应________________________
(3)置换反应________________________
(4)复分解反应________________________
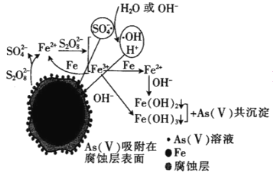
【答案】CaO+H2O=Ca(OH)2 CaCO3![]() CaO+CO2↑ Fe+CuSO4=FeSO4+Cu或3Fe+4H2O(g)
CaO+CO2↑ Fe+CuSO4=FeSO4+Cu或3Fe+4H2O(g) ![]() Fe3O4+4H2 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
Fe3O4+4H2 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
【解析】
(1)CaO和水化合成Ca(OH)2的反应是化合反应,化学方程式为CaO+H2O=Ca(OH)2;
(2)CaCO3受热会分解成CaO和CO2,化学方程式为CaCO3![]() CaO+CO2↑;
CaO+CO2↑;
(3)Fe可以置换出CuSO4中的Cu,也可在高温情况下置换出水的氢,化学方程式为Fe+CuSO4=FeSO4+Cu或3Fe+4H2O(g) ![]() Fe3O4+4H2;
Fe3O4+4H2;
(4)NaOH和CuSO4发生复分解反应得到Cu(OH)2沉淀和Na2SO4,是复分解反应,化学方程式为2NaOH+CuSO4=Cu(OH)2↓+Na2SO4。

【题目】2019年诺贝尔化学奖授予锂离子电池的发明者,LiFePO4是锂离子电池的正极材料。用含锂废渣(主要金属元素的含量:Li 8.50%、Ni 6.55%、Mg 13.24%)制备Li2C2O4,并用其制备LiFePO4部分工艺流程如图(该流程可能造成水体砷污染):
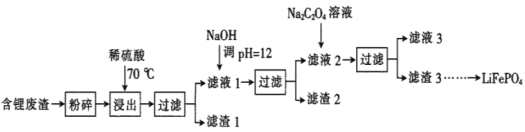
已知:滤液1、滤液2中部分离子的浓度(g·L-1):
Li+ | Ni2+ | Mg2+ | |
滤液1 | 22.72 | 20.68 | 60.18 |
滤液2 | 21.94 | 7.7×10-3 | 0.78×10-3 |
I.制备Li2C2O4
(1)滤渣2的主要成分有__(填化学式)。
(2)Na2C2O4溶液中各离子的浓度由大到小顺序为__。
(3)写出加入Na2C2O4溶液时发生反应的离子方程式:__。
Ⅱ.制备LiFePO4
(4)将电池极Li2C2O4和FePO4置于高温下反应生成LiFePO4和一种温室气体,该反应的化学方程式是___。
(5)LiFePO4需要在高温下成型后才能作为电极,高温成型时要加入少量石墨,则石墨的作用是__(任写一点)。
(6)我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的As(Ⅴ),其机制模型如图,其中零价铁与过硫酸钠反应的离子方程式是__。在该模型中得到的铁砷共沉淀物经灼烧(无元素化合价变化)后得到一种磁性化合物,化学式为Fe7As2O14,该物质中二价铁与三价铁的个数比为__。