题目内容
【题目】电离平衡常数是衡量弱电解质电离程度强弱的量。已知如表数据。
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为__________________。
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)__________c(CH3COO-)(填“>”、“<”或“=”)。
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为___________。
(4)25 ℃时, pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-)=___________。
【答案】Na2CO3溶液>NaCN溶液>CH3COONa溶液 < NaCN+H2O+CO2=HCN+NaHCO3 9.9x10-7 mol/L
【解析】
(1)根据酸的电离常数进行分析判断,电离常数越大,对应盐的水解程度越小,溶液的pH越小;
(2)根据溶液中电荷守恒分析比较;
(3)根据电离平衡常数H2CO3>HCN>HCO3-,结合复分解反应的规律书写方程式;
(4)根据溶液的pH可计算溶液中c(H+)、c(OH-),然后结合电荷守恒计算。
(1)根据图表数据分析,电离常数:CH3COOH>HCN>HCO3-,酸的电离平衡常数越小,其形成的钠盐越容易水解,溶液的碱性就越强。所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度为:Na2CO3溶液>NaCN溶液>CH3COONa溶液;
(2)25 ℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,在该混合溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),若所得溶液显酸性,则c(H+)>c(OH-),所以c(Na+)<c(CH3COO-);
(3)根据表格中的电离平衡常数H2CO3>HCN>HCO3-,可知向NaCN溶液中通入少量CO2,所发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3;
(4)CH3COONa溶液溶液的pH=8,则溶液中c(H+)=10-8mol/L,c(OH-)=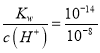 =10-6mol/L,在该混合溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则c(Na+)-c(CH3COO-)= c(OH-)-c(H+)=10-6mol/L-10-8mol/L=9.9×10-7 mol/L。
=10-6mol/L,在该混合溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),则c(Na+)-c(CH3COO-)= c(OH-)-c(H+)=10-6mol/L-10-8mol/L=9.9×10-7 mol/L。

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应