题目内容
下列各组离子,在指定环境中一定能大量共存的是( )
| A、由水电离出的c(OH-)=1×10-13mol/L的溶液中:Fe2+、NH4+、ClO-、Cl- |
| B、能使pH试纸变深蓝色的溶液中:Na+、S2-、SO32-、S2O32- |
| C、加入铝粉能放出氢气的溶液中:Mg2+、AlO2-、I-、NO3- |
| D、pH=7的溶液中:Al3+、K+、SO42-、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.水电离出的c(OH-)=1×10-13mol/L的溶液为酸性或者碱性溶液,溶液中存在大量的氢离子或者氢氧根离子,铵根离子、亚铁离子能够与氢氧根离子反应、次氯酸根离子能够与氢离子、亚铁离子反应;
B.能使pH试纸变深蓝色的溶液为碱性溶液,Na+、S2-、SO32-、S2O32-之间不发生反应,也不与氢氧根离子反应;
C.加入铝粉能放出氢气的溶液为酸性或者碱性溶液,偏铝酸根离子能够与氢离子反应,硝酸根离子在酸性条件下能够氧化碘离子,镁离子能够与氢氧根离子反应;
D.pH=7的溶液为 中性溶液,铝离子与碳酸氢根离子发生双水解反应,且碳酸氢根离子能够水解,溶液显示碱性.
B.能使pH试纸变深蓝色的溶液为碱性溶液,Na+、S2-、SO32-、S2O32-之间不发生反应,也不与氢氧根离子反应;
C.加入铝粉能放出氢气的溶液为酸性或者碱性溶液,偏铝酸根离子能够与氢离子反应,硝酸根离子在酸性条件下能够氧化碘离子,镁离子能够与氢氧根离子反应;
D.pH=7的溶液为 中性溶液,铝离子与碳酸氢根离子发生双水解反应,且碳酸氢根离子能够水解,溶液显示碱性.
解答:
解:A.该溶液为酸性或者碱性溶液,碱性溶液中,Fe2+、NH4+能够与氢氧根离子反应,酸性溶液中,ClO-能够与H+、Fe2+发生反应,在溶液中不能大量共存,故A错误;
B.该溶液为碱性溶液,溶液中存在大量的氢氧根离子,Na+、S2-、SO32-、S2O32-之间不反应,也不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.该溶液为酸性或者碱性溶液,Mg2+能够与氢氧根离子反应生成氢氧化镁沉淀,AlO2-能够与氢离子发生反应,在酸性条件下NO3-能够氧化I-,在溶液中不能大量共存,故C错误;
D.Al3+、HCO3-能够发生双水解反应生成二氧化碳气体和氢氧化铝沉淀,且碳酸氢根离子水解溶液显示碱性,溶液的pH大于7,故D错误;
故选B.
B.该溶液为碱性溶液,溶液中存在大量的氢氧根离子,Na+、S2-、SO32-、S2O32-之间不反应,也不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.该溶液为酸性或者碱性溶液,Mg2+能够与氢氧根离子反应生成氢氧化镁沉淀,AlO2-能够与氢离子发生反应,在酸性条件下NO3-能够氧化I-,在溶液中不能大量共存,故C错误;
D.Al3+、HCO3-能够发生双水解反应生成二氧化碳气体和氢氧化铝沉淀,且碳酸氢根离子水解溶液显示碱性,溶液的pH大于7,故D错误;
故选B.
点评:本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,“加入铝粉产生氢气”.

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
下列关于有机物的说法中不正确的是( )
| A、甲烷与氯气在光照条件下的反应和乙酸与乙醇生成乙酸乙酯的反应均属于取代反应 |
| B、顺-2-丁烯和反-2-丁烯的熔、沸点不相同 |
| C、C4H9Br的同分异构体有4种 |
| D、乙烯、苯、乙酸分子中的所有原子都在同一平面上 |
x、Y为同周期的主族元素,如果X的原子半径大于Y的原子半径,则下列判断中不正确的是( )
| A、若X、Y均为金属元素,则X的金属性比y强 |
| B、若X、Y均为非金属元素,则X的非金属性比Y弱 |
| C、若x为金属,Y为非金属,则X的离子半径比Y的离子半径小 |
| D、若X、Y均为非金属元素,则X原子的氧化性比Y原子强 |
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核才有NMR现象.试判断下列哪组原子均可产生NMR现象( )
| A、18O、31P、119Sn | ||||||
| B、27Al、19F、12C | ||||||
| C、14N、18O、75As | ||||||
D、
|
铅蓄电池的两极分别是Pb、PbO2,电解质溶液为30%硫酸,工作时反应为:Pb+PbO2+2H2SO4
2PbSO4+2H2O当其放电时,下列结论正确的是( )
| 放电 |
| 充电 |
| A、PbO2为正极,被氧化 |
| B、电池电解质溶液的密度不断减小 |
| C、c(H+)逐渐增大 |
| D、H+向负极移动 |
在C(s)+H2O(g)?CO(g)+H2(g)△H>0中,采取下列措施,能使正反应速率增大的措施是( )
①缩小体积,增大压强 ②增加碳的量 ③恒容通入CO ④恒容充入N2 ⑤恒压充入N2⑥降低温度.
①缩小体积,增大压强 ②增加碳的量 ③恒容通入CO ④恒容充入N2 ⑤恒压充入N2⑥降低温度.
| A、①④ | B、②③⑤⑥ |
| C、①③ | D、①②④ |
下列实验操作完全正确的是( )
| A、氢氧化钠贮存在带玻璃塞的试剂瓶中 |
| B、用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
| C、量筒取5.0mL 1mol?L-1 HCl于50mL容量瓶中,加水至刻度可配制0.1mol?L-1盐酸 |
| D、在苯萃取溴水中的溴,分液时有机层从分液漏斗的上口倒出 |
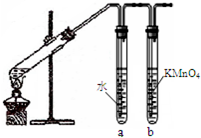 为检验利用溴乙烷发生消去反应后生成的气体中是否含乙烯的装置如图所示.回答:
为检验利用溴乙烷发生消去反应后生成的气体中是否含乙烯的装置如图所示.回答: