题目内容
【题目】氮是一种重要的元素,其对应化合物在生产生活中有重要的应用。
(1)氮化铝(AlN)可用于制备耐高温的结构陶瓷,遇强碱会腐蚀,写出AlN与氢氧化钠溶液反应的离子方程式_____。
(2)氨是制备氮肥、硝酸等的重要原料
①已知:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
N2(g)+O2(g) ![]() 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol
2H2(g)+O2(g) ![]() 2H2O(1) △H= -571.6 kJ/mol
2H2O(1) △H= -571.6 kJ/mol
试写出表示氨的标准燃烧热的热化学方程式_____。
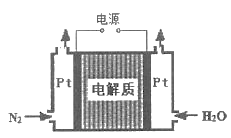
②某电解法制氨的装置如图所示,电解质只允许质子通过,试写出阴极的电极反应式_____。
(3)反应:2NO(g)+O2(g) ![]() 2NO2(g)△H<0 是制备硝酸过程中的一个反应。
2NO2(g)△H<0 是制备硝酸过程中的一个反应。
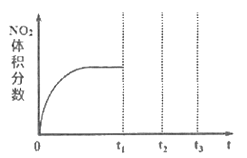
①将NO和O2按物质的量之比为 2:1 置于恒温恒容密闭容器中进行上述反 应,得到NO2 体积分数与时间的关系如图所示。保持其它条件不变,t1 时再向 容器中充入适量物质的量之比为2:1的NO和O2的混合气体,t2 时再次达到平 衡,请画出 tl-t3 时间范围内 NO2 体积分数随时间的变化曲线:_________。
②在研究此反应速率与温度的关系时发现,NO 转化成 NO2 的速率随温度升高反而减慢。进一步研究发现,上述反应实际是分两步进行的:
I.2NO(g) ![]() N2O2(g) △H<0
N2O2(g) △H<0
II.N2O2(g)+O2(g) ![]() 2NO2(g) △H<0
2NO2(g) △H<0
已知反应I能快速进行,试结合影响化学反应速率的因素和平衡移动理论分析,随温度升高,NO 转化成 NO2 的速率减慢的可能原因________。
(4)已知常温下,Ka(CH3COOH)=Kb(NH3·H2O)=l.8×l0-5。则常温下 0.lmol/L 的 CH3COONH4 溶液中,c(CH3COO-):c(NH3·H2O)=_____。
【答案】AlN+H2O+OH-=AlO2-+NH3↑ NH3(g)+![]() O2(g)=
O2(g)=![]() N2(g)+
N2(g)+![]() H2O(l) △H=-382.5kJ·mol-1 N2 + 6H++6e-=2NH3
H2O(l) △H=-382.5kJ·mol-1 N2 + 6H++6e-=2NH3 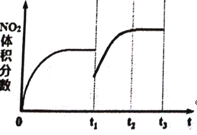 当温度升高时,反应I向逆反应方向进行,且由于反应 I 进行速率相当快, 瞬间达到平衡,使得体系中 c(N2O2)浓度迅速减小,所以反应(II),速率减慢 180
当温度升高时,反应I向逆反应方向进行,且由于反应 I 进行速率相当快, 瞬间达到平衡,使得体系中 c(N2O2)浓度迅速减小,所以反应(II),速率减慢 180
【解析】
(1)AlN能与强碱发生反应,Al元素转变成AlO2-,即离子方程式为AlN+H2O+OH-=AlO2-+NH3↑;
(2)①氨的标准燃烧热的方程式为NH3(g)+![]() O2(g)=
O2(g)=![]() N2(g)+
N2(g)+![]() H2O(l),①N2(g)+3H2(g)
H2O(l),①N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ·mol-1,②2H2(g)+O2(g)
2NH3(g) △H=-92.4kJ·mol-1,②2H2(g)+O2(g) ![]() 2H2O(1) △H= -571.6 kJ·mol-1,根据盖斯定律,
2H2O(1) △H= -571.6 kJ·mol-1,根据盖斯定律,![]() ,得出△H=-382.5kJ·mol-1,即热化学反应方程式为NH3(g)+
,得出△H=-382.5kJ·mol-1,即热化学反应方程式为NH3(g)+![]() O2(g)=
O2(g)=![]() N2(g)+
N2(g)+![]() H2O(l) △H=-382.5kJ·mol-1;
H2O(l) △H=-382.5kJ·mol-1;
②电解法制备氨,装置的左侧N2→NH3,N的化合价降低,左侧为阴极,右侧为阳极,电解质只允许质子通过,即阴极反应式为N2+6H++5e-=2NH3;
(3)①达到平衡后,再充入2:1的NO和O2的混合气体,瞬间NO2的体积分数降低,平衡向正反应方向移动,NO2的体积分数增大,由于是恒容充入物质的量之比与原来相同的NO和O2的混合气体,总体上相当于增大压强,即达到平衡时,NO2的体积分数比原平衡高,图像为 ;
;
②本题考查影响化学反应速率和化学平衡的因素,当温度升高时,反应I向逆反应方向进行,且由于反应 I 进行速率相当快, 瞬间达到平衡,使得体系中 c(N2O2)浓度迅速减小,所以反应(II),速率减慢;
(4)因为醋酸和NH3·H2O电离平衡常数相同,因此CH3COO-和NH4+![]() ,变形得到:
,变形得到:![]() =180。
=180。

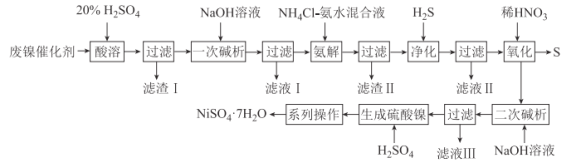
【题目】PbCO3广泛用于陶瓷、油漆和颜料配制等。一种由方铅矿(主要成分为PbS,含少量FeS)和软锰矿(主要成分为MnO2)为原料制备PbCO3的流程如图:
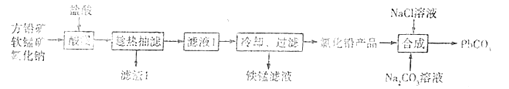
已知:①“酸浸”时PbS反应的方程式为PbS+MnO2+4Cl-+4H+=== PbCl42-+Mn2++S+2H2O。PbCl2易溶于热水,难溶于冷水。在盐酸中因与Cl-形成配合离子PbCl42-而增大PbCl2的溶解度.
②常温下,几种金属离子沉淀的pH如表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
开始沉淀的pH | 1.5 | 7.5 | 8.8 |
完全沉淀的pH | 2.3 | 9.7 | 10.4 |
(1)“酸浸”之前需要将方铅矿、软锰矿和氧化钠粉碎并混合均匀,其目的是____。
(2)“趁热抽滤”的目的是___。
(3)铁锰滤液中阳离子主要是Mn2+,还含少量Fe3+、Fe2+。从铁锰滤液中得到较纯锰盐溶液有两种方案:
方案甲:向滤液中加入酸化的双氧水,再加入足量MnCO3粉末,过滤得到锰盐溶液。
方案乙:向滤液中加入稀硫酸酸化,然后加入二氧化锰粉末,充分反应;最后,加氨水调节溶液pH,过滤。
①方案甲中加入MnCO3的目的是_____。
②用离子方程式表示方案乙中“加入二氧化锰”的作用:____。
已知常温下,Ksp[Fe(OH)3]≈1.0×10-38,为了使溶液中c(Fe3+)=1.0×10-5mol·L-1,此时溶液的pH= ____。
③从操作、产品纯度角度考虑,方案____(填“甲”或”乙”)优于另一种方案。
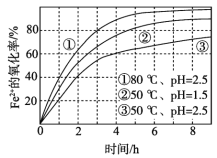
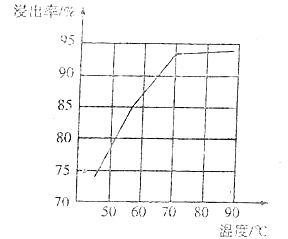
(4)研究工业生产中温度对浸出率的影响如图所示,则生产中浸出过程的最佳温度是___。
(5)向氯化铅(难溶于水)产品中加入氯化钠溶液和碳酸钠溶液,得到碳酸铅产品后,要经过“过滤、洗涤、干燥”等操作,检验碳酸铅是否洗涤干净的操作是____。