题目内容
【题目】在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g)![]() 2C(g) ΔH<0,某时刻达到平衡后,在
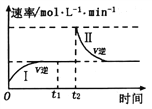
2C(g) ΔH<0,某时刻达到平衡后,在![]() 时刻改变某一条件,其反应过程如图所示。下列说法正确的是( )
时刻改变某一条件,其反应过程如图所示。下列说法正确的是( )
A. ![]()
B. I、Ⅱ两过程达到平衡时,A的体积分数I>II
C. ![]() 时刻改变的条件是向密闭容器中加C
时刻改变的条件是向密闭容器中加C
D. I、II两过程达到平衡时,平衡常数I<II
【答案】C
【解析】试题分析:A、根据图像可知反应进行到t1时就已经达到平衡状态,此时正逆反应速率相等,A错误;B、t2 时刻逆反应速率瞬间增大,然后逐渐减小,最后恢复到原来的速率,这说明平衡不移动,所以I、Ⅱ两过程达到平衡时,A的体积分数I=II,B错误;C、由于反应前后体积不变,且容器体积可知,因此B中分析可知t2 时刻改变的条件是向密闭容器中加C,C正确;D、平衡常数只与温度有关系,则I、II两过程达到平衡时,平衡常数I=II,D错误,答案选C。

【题目】在某温度T℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中,反应过程中浓度变化如下[2NO2(g)![]() N2O4(g) △H<0]:
N2O4(g) △H<0]:
容器 | 物质 | 起始浓度/(mol | 平衡浓度/(mol |
Ⅰ | N2O4 | 0.100 | 0.040 |
NO2 | 0 | 0.120 | |
Ⅱ | N2O4 | 0 | 0.0142 |
NO2 | 0.100 | 0.0716 |
下列说法不正确的是( )
A. 平衡时,Ⅰ、Ⅱ中反应的转化率a(N2O4)>a(NO2)
B. 平衡后,升高相同温度,以N2O4表示的反应速率v(Ⅰ)<v(Ⅱ)
C. 平衡时,Ⅰ、Ⅱ中正反应的平衡常数K(I)=![]()
D. 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
【题目】下列说法正确的是( )
A. KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
B. 向Cr2O72- + H2O![]() 2CrO42-+ 2H+ 的平衡体系中滴加10~20滴6mol/LNaOH溶液颜色由橙色变黄色
2CrO42-+ 2H+ 的平衡体系中滴加10~20滴6mol/LNaOH溶液颜色由橙色变黄色
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为 N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
D. 已知:
共价键 | C-C | C=C | C-H | H-H |
键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
则可以计算出反应 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1