题目内容
16.下列说法正确的是( )| A. | 向0.1mol•L-1氨水中加入适量NH4Cl(s),则混合液中c(NH4+)与c(NH3•H2O)之比增大 | |
| B. | 25℃时,0.1mol•L-1氨水和0.05 mol•L-1氨水中c(OH-)之比是2:1 | |
| C. | 0.1mol•L-1 CH3COOH溶液中,c(CH3COO-)=c(H+) | |
| D. | 向0.1mol•L-1KNO3溶液中,滴加稀盐酸至溶液pH=5,此时混合液中c(K+)<c(NO3-) |
分析 A.加入氯化铵后溶液中铵根离子浓度增大,氢氧根离子浓度减小,然后结合氨水的电离平衡常数判断;
B.弱电解质溶液中,浓度越小,弱电解质的电离程度越大;
C.根据醋酸溶液中的电荷守恒判断;
D.根据硝酸钾溶液中的物料守恒分析.
解答 解:A.向0.1mol•L-1氨水中加入适量NH4Cl(s),一水合氨的电力平衡向着逆向移动,溶液中氢氧根离子浓度减小,根据Kb=$\frac{c(N{{H}_{4}}^{+})•c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$可知,温度不变、Kb不变,则混合液中c(NH4+)与c(NH3•H2O)之比=$\frac{{K}_{b}}{c(O{H}^{-})}$的比值增大,故A正确;
B.25℃时,如果一水合氨是强电解质,则0.1 mol•L-1氨水和0.05mol•L-1 氨水中c(OH-)之比是2:1,实际上,一水合氨是弱电解质且溶液浓度越稀,一水合氨的电离程度越大,所以0.1 mol•L-1氨水和0.05mol•L-1 氨水中c(OH-)之比小于2:1,故B错误;
C.0.1mol•L-1 CH3COOH溶液中存在电荷守恒:c(CH3COO-)+c(OH-)=c(H+),则c(CH3COO-)<c(H+),故C错误;
D.混合液中硝酸根离子和钾离子都不反应,根据物料守恒可知:c(K+)=c(NO3-),故D错误;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理及其影响危机的关键,注意掌握电荷守恒、物料守恒及盐的水解原理在判断离子浓度大小中的应用方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
10.下列说法错误的是( )
| A. | 化合反应不一定是氧化还原反应 | |
| B. | 置换反应一定是氧化还原反应 | |
| C. | 氧化还原反应中,非金属单质一定是氧化剂 | |
| D. | 氧化还原反应中,金属单质一定是还原剂 |
11.在t℃时,将0.2mol X和0.8mol Y充入密闭容器中,当反应X(g)+Y(g)?nZ(g)+R(g)达到平衡时,若将反应混合气体中各物质浓度均增大一倍,X的转化率不变,并知c(X)c(Y)=c(Z)nc(R),则X的转化率为( )
| A. | 80% | B. | 65% | C. | 45% | D. | 37% |
1.具备基本的化学实验技能是进行科学探究的保证.下列实验操作中正确的是( )
| A. | 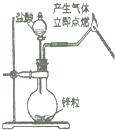 验证氢气的可燃性 | B. |  闻气体气味 | ||
| C. | 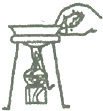 移走蒸发皿 | D. | 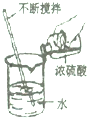 稀释浓硫酸 |
8.在下列各说法中,正确的是( )
| A. | 热化学方程式中的化学计量数只表示物质的量,可以是分数 | |
| B. | △H>0表示放热反应,△H<0表示吸热反应 | |
| C. | 1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 | |
| D. | 1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 |
5.下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中 ②过量Ba(OH)2浓溶液和AlNH4(SO4)2溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中
⑤Na2S2O3溶液中加入稀硫酸.
①金属钠投入到FeCl3溶液中 ②过量Ba(OH)2浓溶液和AlNH4(SO4)2溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中 ④Na2O2投入FeCl2溶液中
⑤Na2S2O3溶液中加入稀硫酸.
| A. | 只有①②④⑤ | B. | 只有③ | C. | 只有②③ | D. | 只有①④⑤ |
6.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A. | 将石灰石加入新制氯水中,固体逐渐溶解(H+) | |
| B. | 向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2) | |
| C. | 使红色布条褪色(HCl) | |
| D. | 滴加AgNO3溶液生成白色沉淀(Cl-) |

 )就是其中的一种.
)就是其中的一种.