题目内容
关于钢铁腐蚀与防护的说法不正确的是
| A.钢铁的吸氧腐蚀和析氢腐蚀的负极反应式均为:Fe-2e-= Fe2+ |
| B.钢铁发生吸氧腐蚀时,正极反应式为:O2+2H2O+4e-= 4OH- |
| C.地下钢管连接镁块是采用牺牲阳极的阴极保护法 |
| D.用外加电流的阴极保护法防止钢铁腐蚀时,钢铁接电源的正极 |
D
解析试题分析:A、发生腐蚀时,活泼的金属作负极,不如负极活泼的金属或导电的非金属作正极,所以铁作负极,氧气作正极,负极失电子变成离子进入溶液,负极反应为Fe-2e-= Fe2+;B、正极上得电子发生还原反应,故吸氧腐蚀时正极反应O2+2H2O+4e-= 4OH-C、牺牲阳极的阴极保护法:其原理是利用原电池原理对金属进行防护,其方法是:将被保护的金属作为原电池的正极,将比被保护金属活泼的另一种金属作为原电池的负极,镁比铁活泼作为阳极保护阴极铁,故C正确;D、外加电流的阴极保护法:其原理是利用电解池原理对金属进行防护,其方法是:将被保护的金属作为电解池的阴极,用惰性电极作为辅助阳极,两者均存在于电解质溶液中,接上外加直流电源,钢铁应作为阴极连接电源负极,故D错误。
考点:金属的电化学腐蚀与防护

观察下列几个装置示意图,有关叙述正确的是:
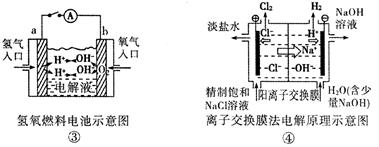
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源正极相连 |
| C.装置③闭合电键后,外电路电子由a极流向b极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
下列有关金属的说法正确的是( )
| A.不锈钢不易生锈是因为表面有致密保护层 |
| B.纯银的器皿在空气中久置表面变暗是因为发生电化学腐蚀 |
| C.当镀锌铁制品的镀层破损时,镀层还能对铁制品起保护作用 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
最近有研究人员发现了一种处理高浓度乙醛废水的新方法— 隔膜电解法,乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸。实验室以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。下列说法正确的是 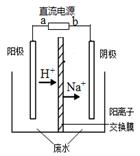
| A.若以CH4—空气燃料电池为直流电源,燃料电池的b极应通入空气 |
| B.电解过程中,阴极区Na2SO4的物质的量增大 |
| C.阳极反应CH3CHO -2e- + 2H+="=" CH3COOH + H2O |
| D.电解过程中,两极除分别生成乙酸和乙醇外,均产生了无色气体,则阳极产生的是O2 |
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化铁制备金属钛。下列说法中正确的是
| A.将熔融CaF2-CaO换成Ca(NO3)2溶液也可以达到相同目的 |
B.阳极的电极反应式为:C+2O2--4e- CO2↑ CO2↑ |
| C.在制备金属钛前后,整套装置中CaO的总量减少 |
| D.若用铅蓄电池作该装置的供电电源,“+"接线柱应连接Pb电极 |
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极,②④相连时,②有气泡逸出;③④相连时,③的质量减少,据此判断这四种金属活动性由大到小的顺序是
| A.①③②④ | B.①③④② | C.③④②① | D.③①②④ |
关于铜电极的叙述中不正确的是
| A.铜锌原电池中铜是正极 |
| B.在镀件上镀铜时可用金属铜作阳极 |
| C.用电解法精炼铜时粗铜做阳极 |
| D.用电解法精炼铜时纯铜做阳极 |
如图所示,电解未精制饱和食盐水(含有少量Mg2+),在碳棒和铁片表面均有气体生成,一段时间后铁片附近出现浑浊现象。下列叙述正确的是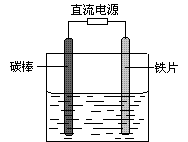
| A.碳棒接直流电源的负极 |
| B.碳棒上发生还原反应 |
| C.铁片上的电极反应式为2Cl――2e- = Cl2↑ |
| D.铁片附近出现的浑浊物是Mg(OH)2 |
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越
来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为xMg+Mo3S4 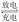 MgxMo3S4;在镁原电池放电时,下列说法错误的是
MgxMo3S4;在镁原电池放电时,下列说法错误的是
| A.Mg2+向正极迁移 |
| B.正极反应为:Mo3S4+2xe-=Mo3S42x- |
| C.Mo3S4发生氧化反应 |
| D.负极反应为:xMg-2xe-=xMg2+ |