题目内容
将3.48gFe3O4完全溶解于100mL0.5mol/L硫酸中,然后加入K2Cr2O7溶液25mL ,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72-全部还原为Cr3+,则K2Cr2O7溶液的物质的量浓度为
| A.0.05mol/L | B.0.1mol/L | C.0.2mol/L | D.0.3mol/L |
B
3.48gFe3O4完全溶解于100mL0.5mol/L硫酸中,会得到0.015molFe2+
14H++6Fe2++Cr2O72-=6Fe3++2Cr3++7H2O
6 1
0.015 X
列比例式得到X=0.0025mol,C(K2Cr2O7)= 0.1mol/L 故选B。
14H++6Fe2++Cr2O72-=6Fe3++2Cr3++7H2O
6 1
0.015 X
列比例式得到X=0.0025mol,C(K2Cr2O7)= 0.1mol/L 故选B。

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
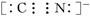 。它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O
。它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O 2K2SO4+FeSO4+3(NH4)2SO4+6CO↑
2K2SO4+FeSO4+3(NH4)2SO4+6CO↑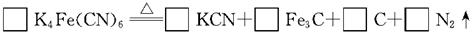

 述反应中的氧化剂是______。
述反应中的氧化剂是______。