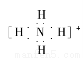题目内容
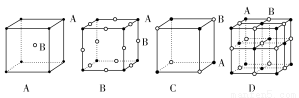
以下有关杂化轨道的说法中错误的是( )
A.ⅠA族元素成键时不可能有杂化轨道
B.杂化轨道既可能形成σ键,也可能形成π键
C.孤对电子有可能参加杂化
D.s轨道和p轨道杂化不可能有sp4出现
B
【解析】ⅠA族元素的价电子排布为ns1,由于只有1个ns电子,因此不可能形成杂化轨道;杂化轨道之间的重叠均是“头碰头”式,只形成σ键;在H2O分子和NH3分子中的氧原子和氮原子,均是采取sp3杂化,其sp3杂化轨道分别有2个和1个由孤对电子占据,孤对电子有可能参加杂化的说法是对的;由于np能级只有3个原子轨道,所以s轨道和p轨道杂化只有sp3、sp2、sp三种,不可能出现sp4。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7%,O2 11%,N2 82%):
压强/MPa 转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
400 | 99.2 | 99.6 | 99.7 | 99.9 |
500 | 93.5 | 96.9 | 97.8 | 99.3 |
600 | 73.7 | 85.8 | 89.5 | 96.4 |
(1)已知SO2的氧化是放热反应,如何利用表中数据推断此结论?________________________________________________________。
(2)在400~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:__________________________________________。
(3)选择适宜的催化剂,是否可以提高SO2的转化率?________(填“是”或“否”),是否可以增大该反应放出的热量?________(填“是”或“否”)。
(4)为提高SO3吸收率,实际生产中用________吸收SO2。
(5)已知:2SO2(g)+O2(g)=2SO3(g) ΔH=-196.9 kJ·mol-1,计算每生产1万吨98%的硫酸所需要的SO3质量和由SO2生产这些SO3所放出的热量。