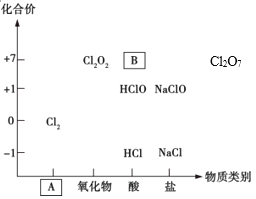
题目内容
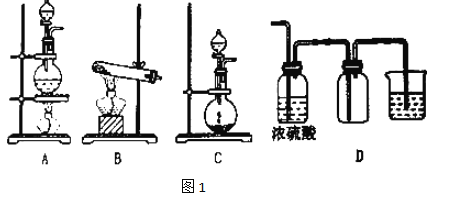
【题目】某兴趣小组设计如下图实验装置进行实验。
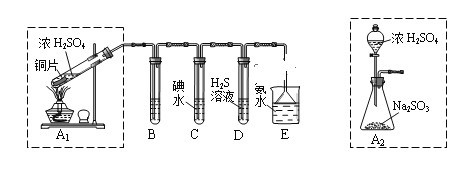
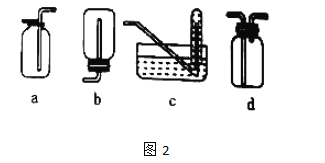
(1)为了实现绿色环保的目标,能否用上图A2代替A1装置______(填“能”或“否”)。
(2)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为____________
C中反应的离子方程式为__________________________,D中反应的化学方程为___________________。
(3)氨水吸收过量SO2的反应的离子方程式为__________________________________________
【答案】能 品红溶液 SO2+I2+2H2O=SO42-+2I-+4H+ SO2+2H2S=3S↓+2H2O NH3·H2O+SO2=NH4++HSO3-
【解析】
(1) Na2SO3+H2SO4(浓)==Na2SO4+H2O+SO2↑,也是实验室制SO2的方法之一。
(2)B用于检验SO2的漂白性,则B中所盛试剂为品红溶液。
C中反应为SO2与碘水反应,生成硫酸和氢碘酸两种强酸,D中反应为SO2与H2S反应,生成硫和水。
(3)氨水吸收过量SO2时,应生成NH4HSO3。
(1)因为实验室也可用以下反应制取二氧化硫:Na2SO3+H2SO4(浓)==Na2SO4+H2O+SO2↑,所以为了实现绿色环保的目标,能用上图A2代替A1装置。答案为:能;
(2)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为品红溶液,C中反应的离子方程式为SO2+I2+2H2O=SO42-+2I-+4H+,D中反应的化学方程为SO2+2H2S=3S↓+2H2O。答案为:品红溶液;SO2+I2+2H2O=SO42-+2I-+4H+;SO2+2H2S
=3S↓+2H2O;
(3)氨水吸收过量SO2的反应的离子方程式为NH3·H2O+SO2=NH4++HSO3-。答案为:NH3·H2O+SO2=NH4++HSO3-。

【题目】现有五种有机物,请回答下列问题:
A. | B. | C. |
D.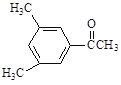 E.
E.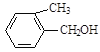 F.
F.![]()
(1)A物质中含有的官能团名称为_____________、______________。
(2)B的分子式为_________________。
(3)D的一氯代物最多有________________种。
(4)上述化合物中互为同分异构体的是_____;互为同系物的是____。(填字母)