��Ŀ����
����Ŀ����ҵˮ�ϼ�̼��þ�������̼��þ��3MgCO3.Mg(OH)2.3H2O��������ܶ�С��������ɣ��㷺��������Ʒ������ʪ���Ϻ��ջ���Ʒ�еȡ�һ���Ը����Ȼ�þ������þ��±ˮ�Ͱ���ʯ��CaMg(CO3)2��Ϊԭ�ϵ�±ˮ̼������������̼��þ�Ĺ����������£�
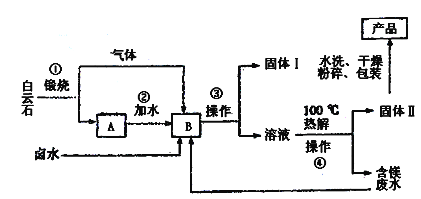
��֪��MgCO3��CaCO3������CO2��Ӧ���ɿ������Ρ�
��1��Ϊ��ʹ�ڢٲ�����ʯ���յø���֣�����Ҫ�Կ�ʯ����__Ԥ������
��2���ڢ۲��͵ڢܲ�������������__����ʵ���ҽ��иò���ʱ��Ҫ�IJ���������
__��
��3������I����Ҫ�ɷ�Ϊ____������II����Ҫ�ɷ�Ϊ____��ˮϴ����IIʱ������ж��Ѿ�ϴ�������������̣�____��
��4��д���ڢܲ���Ӧ�Ļ�ѧ����ʽ��____��
��5������������ͬ�������Ч�桢���ٷ����ŷ�˼������������____��
���𰸡� ���� ���� ©�����ձ��������� CaCO3 3MgCO3��Mg(OH)2��3H2O ȡ����ϴ��Һ���Թ��У�����HNO3�ữ��AgNO3��Һ����û�а�ɫ�������ɣ�����ϴ������֮��δϴ�� 4Mg(HCO3)2![]() 3MgCO3��Mg(OH)2��3H2O+5CO2�� �����հ���ʯ������CO2�ͺ�þ��ˮ����B��
3MgCO3��Mg(OH)2��3H2O+5CO2�� �����հ���ʯ������CO2�ͺ�þ��ˮ����B��
��������������Ҫ�������±ˮ̼������������̼��þ�Ĺ������̵����ۡ�
��1��Ϊ��ʹ�ڢٲ�����ʯ���յø���֣�����Ҫ�Կ�ʯ���з���Ԥ������
��2���ڢ۲��͵ڢܲ������õ��������Һ���������ǵ������ǹ��ˣ���ʵ���ҽ��иò���ʱ��Ҫ�IJ���������©�����ձ�����������
��3��MgCO3��CaCO3������CO2��Ӧ���ɿ������Σ�����I����Ҫ�ɷ�ΪCaCO3������II����Ҫ�ɷ־��Dz�Ʒ����Ҫ�ɷ�Ϊ3MgCO3��Mg(OH)2��3H2O������II��������±ˮ������Cl����![]() �����ӣ��ж�ˮϴ����II�Ƿ��Ѿ�ϴ���������ж�������Cl����
�����ӣ��ж�ˮϴ����II�Ƿ��Ѿ�ϴ���������ж�������Cl���� ![]() �Ƿ��Ѿ�ϴ�������Լ���Cl��������̣�ȡ����ϴ��Һ���Թ��У�����HNO3�ữ��AgNO3��Һ����û�а�ɫ�������ɣ�����ϴ������֮��δϴ����
�Ƿ��Ѿ�ϴ�������Լ���Cl��������̣�ȡ����ϴ��Һ���Թ��У�����HNO3�ữ��AgNO3��Һ����û�а�ɫ�������ɣ�����ϴ������֮��δϴ����
��4���ڢܲ���Ӧ�Ļ�ѧ����ʽ��4Mg(HCO3)2![]() 3MgCO3��Mg(OH)2��3H2O+5CO2����
3MgCO3��Mg(OH)2��3H2O+5CO2����
��5������������ͬʱ�������Ч�桢���ٷ����ŷ�˼�����������ǰ����հ���ʯ������CO2�ͺ�þ��ˮ����B�С�