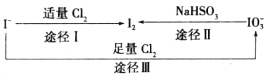
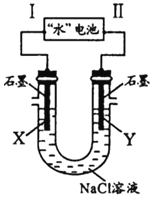
题目内容
【题目】已知:(1)Zn(s)+1/2O2(g)==ZnO(s),ΔH=-348.3kJ/mol
(2)2Ag(s)+1/2 O2(g)=Ag2O(s),ΔH=-31.0kJ/mol
则Zn(s)+ Ag2O(s)=ZnO(s)+ 2Ag(s)的ΔH等于( )
A.-317.3kJ/mol B.-379.3kJ/mol C.-332.8 kJ/mol D.317.3 kJ/mol
【答案】A
【解析】
试题分析:由(1)Zn(s)+![]() O2(g)=ZnO(s)△△H=-348.3kJ/mol,
O2(g)=ZnO(s)△△H=-348.3kJ/mol,
(2)2Ag(s)+![]() O2(g)=Ag2O(s)△H=-31.0kJ/mol,根据盖斯定律可知,
O2(g)=Ag2O(s)△H=-31.0kJ/mol,根据盖斯定律可知,
(1)-(2)可得Zn(s)+Ag2O(s)═ZnO(s)+2Ag(s),
则△H=(-348.3kJmol-1)-(-31.0kJmol-1)=-317.3kJmol-1,故选A。

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目