题目内容
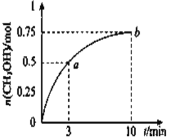
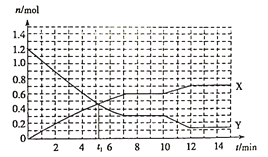
【题目】某溶液中可能含有H+、Na+、NH4+、Fe3+、Al3+、SO42-、CO32-等离子。向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图像如图所示。

(1)A、B、C、D四点中沉淀成分相同的是(写代号)_______________
(2)由图像可推出原溶液中一定含有的离子有:____________________
(3)若要检验可能存在的离子应采取的方法是______________________
(4)原溶液中含有的Fe3+和Al3+的物质的量之比为______________
(5)由图像计算使用的NaOH溶液的物质的量浓度是________________
【答案】B、C点 H+、NH4+、Fe3+、Al3+、SO42- 利用焰色反应判断,焰色反应呈黄色,证明含有钠离子 1:1 1mol/L
【解析】
根据图象中最初没有沉淀可知,一定有H+;CD段,生成的沉淀又溶解了一部分,可知一定有Al3+,BC段,和氢氧化钠反应不产生沉淀,说明有NH4+,根据坐标可知氢氧化铝溶解用了1L的氢氧化钠,生成沉淀用了6L的氢氧化钠,所以形成氢氧化铝用了3L的氢氧化钠,还有3L的氢氧化钠一定是和Fe3+反应,所以一定含有Fe3+,则一定不含CO32-,即原溶液中一定含有的阳离子有H+、NH4+、Fe3+、Al3+;由于溶液呈电中性,则一定有SO42-;Na+可能存在;
(1)A、B、C、D四点中沉淀成分相同的是B、C点;
(2)原溶液中一定含有的离子有:H+、NH4+、Fe3+、Al3+、SO42-;
(3)钠离子可能存在,可利用焰色反应判断,焰色反应呈黄色,证明含有钠离子;
(4)根据坐标可知氢氧化铝溶解用了1L的氢氧化钠,生成沉淀用了6L的氢氧化钠,所以形成氢氧化铝用了3L的氢氧化钠,还有3L的氢氧化钠一定是和Fe3+反应,则原溶液中含有的Fe3+和Al3+的物质的量之比为1:1;
(5)根据坐标可知氢氧化铝溶解了1mol用了1L的氢氧化钠,则n(NaOH)=1mol,c(NaOH)=1mol/L。

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案【题目】氮元素的单质和常见的化合物在工、农业生产中用途广泛。
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
N2 | O2 | Ar | CO2 |
-196℃ | -183℃ | -186℃ | -78℃ |
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是______.
(2)雷雨时空气中的N2转化为NO,生成物NO是______色的气体,______(填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应,写出NO2与水反应的化学方程式为__________________.
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气;
①制取氨气的化学方程式为__________________;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为______g;
(4)已知:4NH3+6NO![]() 5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能;
5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能; ![]()
若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同);
①NH3与稀硫酸溶液反应的离子方程式为__________________;
②为了比较不同催化剂的催化性能,需要测量并记录的数据是____________。