题目内容
【题目】如图为原电池装置示意图,
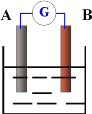
(1)若A为Zn片,B为石墨棒,电解质溶液为稀硫酸,则A电极名称为_________,写出正极的电极反应式______________;
(2)若A为铜片,B为银片,电解质为AgNO3溶液,则银片为______________极(填正或负),写出电极反应式:负极______________,正极______________
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃烧电池,该燃料电池的总反应为______________。
【答案】负极 2H++2e-=H2↑ 正 Cu-2e-=Cu2+ 2Ag++2e-=2Ag 2H2+O2=2H2O
【解析】
(1)若A为Zn片,B为石墨棒,该原电池中,锌失去电子变成锌离子进入溶液,所以锌极(A极)为负极,石墨为正极,正极上氢离子得电子生成氢气,所以电极反应式为2H++2e-=H2↑;
(2)若A为铜片,B为银片,电解质为AgNO3溶液,该原电池中,铜片作负极,铜片失电子变成二价铜离子进入溶液,电极反应式为Cu-2e-=Cu2+;银片作正极,正极上银离子得电子生成银单质,电极反应式为2Ag++2e-=2Ag;
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,在该氢氧燃料电池中,通入氢气的一极为负极,通入氧气的一极为正极,氢气和氧气反应生成水,所以电池总反应式为2H2+O2=2H2O。

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目