��Ŀ����
����Ŀ��Ǧ���������ұ������Ǧ������Ҫ�ɷ�ΪPbS��
��1������Ǧ��Ǧ�����ڿ����б��գ�����PbO��SO2��
����Ǧ�������Ǧ�ķ�Ӧ�Ļ�ѧ����ʽΪ____________________________��
�ڻ���Ǧ�ķ����к���Ũ��SO2���ɽ�����ͨ�������ˮ�н��д�������Ӧ�����ӷ���ʽΪ_____________________________________________________��
��2��ʪ����Ǧ���Ʊ�����Ǧ��ͬʱ�������Ƶ���ǣ�����ڻ���Ǧ��Ϊ������ʪ����Ǧ�Ĺ����������£�

��֪��PbCl2Ϊ������ˮ��������ʣ���Cl-Ũ�Ƚϴ����Һ�У�����ƽ�⣺PbCl2(aq) + 2Cl-(aq) ![]() PbCl42-(aq)����ͬ�¶���PbCl2���ܽ�����±���ʾ��
PbCl42-(aq)����ͬ�¶���PbCl2���ܽ�����±���ʾ��
�¶ȣ��棩 | 20 | 40 | 60 | 80 | 100 |
�ܽ�ȣ�g�� | 1.00 | 1.42 | 1.94 | 2.88 | 3.20 |
�ٽ�ȡҺ��FeCl3��������________________________________��
�ڲ���aΪ������ˮϡ�Ͳ���ȴ���ò�����������Һ1��PbCl2���������������ܵ�ԭ����___________________________________________________________________��
�۽���Һ3����Һ2�ֱ�������ͼ��ʾ���װ�õ����������У�����ȡ����Ǧ��ʹ��ȡҺ�е�FeCl3������

��.��Һ3Ӧ����_________ ��������ҡ��������ҡ����С�
��.������Һ2��������ΪFeCl3��ԭ��______________________________________��
��.��Ǧ���������Ϊa g��Ǧ������Ϊb ����������ͨ��c mol����ʱ������Ǧȫ��������Ǧ������PbS����������Ϊ___________��
���𰸡�2PbS + 3O2![]() 2PbO + 2SO22NH3��H2O + SO2��2NH4+ + SO32- + H2OʹPbԪ�ش����ܹ���PbSת������Һ�е�PbCl4-��SԪ��ת���ɵ������Ϊ������ˮϡ��ʹPbCl2(aq) + 2Cl-(aq)
2PbO + 2SO22NH3��H2O + SO2��2NH4+ + SO32- + H2OʹPbԪ�ش����ܹ���PbSת������Һ�е�PbCl4-��SԪ��ת���ɵ������Ϊ������ˮϡ��ʹPbCl2(aq) + 2Cl-(aq) ![]() PbCl42-(aq)ƽ�������ƶ����¶Ƚ���PbCl2�ܽ�ȼ�С���������������缫��Ӧ��Fe2+- e-
PbCl42-(aq)ƽ�������ƶ����¶Ƚ���PbCl2�ܽ�ȼ�С���������������缫��Ӧ��Fe2+- e- ![]() Fe3+����2Cl--2e-
Fe3+����2Cl--2e-![]() Cl2��Cl2 + 2Fe2+ = 2Fe3+ + 2Cl-�����ֱ���Ҳ�ɣ���ʹc(Fe3+)���ߣ�ͬʱCl-ͨ�������ӽ���Ĥ�������ƶ���ʹFeCl3����
Cl2��Cl2 + 2Fe2+ = 2Fe3+ + 2Cl-�����ֱ���Ҳ�ɣ���ʹc(Fe3+)���ߣ�ͬʱCl-ͨ�������ӽ���Ĥ�������ƶ���ʹFeCl3����![]()
��������
Ǧ����ͨ�������Ȼ������Ȼ�����Һ�Ľ��ݣ����ȣ����ȹ��ˣ��õ����Ȼ�Ǧ���Ȼ�������Һ�ͺ������ʵ���������Һ������ˮϡ�Ͳ���ȴ���õ��Ȼ�������Һ������PbCl2��PbCl2�����Ȼ�����Һ��ʹƽ��PbCl2(aq) + 2Cl-(aq) ![]() PbCl42-(aq)�����ƶ����õ���Һ�������������Ȼ�������Һ��ͬ��ɵ��أ����õ�Ǧ���ʺͺ����Ȼ�������Һ��
PbCl42-(aq)�����ƶ����õ���Һ�������������Ȼ�������Һ��ͬ��ɵ��أ����õ�Ǧ���ʺͺ����Ȼ�������Һ��
(1)�����⣬Ǧ�����ڿ����б��գ�����PbO��SO2�ͣ�����������Ӧ���ʷ�Ӧ����ʽΪ��2PbS + 3O2![]() 2PbO + 2SO2�� (2)�����������������壬��ˮ�Լ��ԣ��ð�ˮ�����ն������õ���Ӧ����κ�ˮ�����ӷ���ʽΪ��2NH3��H2O + SO2��2NH4+ + SO32- + H2O �� (3)��ȡҺ���Ȼ���������������Ũ�ȣ���������Ũ�Ƚϴ�ʱ����Һ�д���ƽ��PbCl2(aq) + 2Cl-(aq)
2PbO + 2SO2�� (2)�����������������壬��ˮ�Լ��ԣ��ð�ˮ�����ն������õ���Ӧ����κ�ˮ�����ӷ���ʽΪ��2NH3��H2O + SO2��2NH4+ + SO32- + H2O �� (3)��ȡҺ���Ȼ���������������Ũ�ȣ���������Ũ�Ƚϴ�ʱ����Һ�д���ƽ��PbCl2(aq) + 2Cl-(aq) ![]() PbCl42-(aq)�������ƶ��� ʹPbԪ������ʽ������Һ�У����������Ӿ��������ԣ������Ӿ��л�ԭ�ԣ�����������ԭ��Ӧ��ʹ��Ԫ��ת��Ϊ�������Ϊ������ (4). PbCl2Ϊ������ˮ��������ʣ�����ƽ��PbCl2(aq) + 2Cl-(aq)
PbCl42-(aq)�������ƶ��� ʹPbԪ������ʽ������Һ�У����������Ӿ��������ԣ������Ӿ��л�ԭ�ԣ�����������ԭ��Ӧ��ʹ��Ԫ��ת��Ϊ�������Ϊ������ (4). PbCl2Ϊ������ˮ��������ʣ�����ƽ��PbCl2(aq) + 2Cl-(aq) ![]() PbCl42-(aq)����ˮϡ�ͣ�������Ũ�Ƚ��ͣ�ƽ�������ƶ�����ȴ���¶Ƚ��ͣ� PbCl2�ܽ�ȼ�С���Ӷ�����PbCl2���塣(5) ����Һ3�Ǻ���PbCl42-����Һ��Ҫ�Ƶõ���Ǧ��Ԫ��Ǧ�Ļ��ϼ۽��ͣ��õ����ӣ�������ԭ��Ӧ�����ݵ��صĹ���ԭ���������õ����ӣ�����Һ3Ӧ���������ҡ�������������Һ2����Һ2���Ȼ�������Һ����������������ʧȥ���ӣ�ת��Ϊ�����ӣ��缫��Ӧ��Fe2+- e-= Fe3+��ʹc(Fe3+)���ߣ���Һ�е�������������ͨ�������ӽ���Ĥ���ﵽ�����ң��������ӽ�ϣ��õ��Ȼ���������Pb2+--Pb��1mol Pb2+ת��2mol���ӣ���������ͨ��cmol����ʱ������Ǧȫ�����������Ծ���c/2mol��Ǧ������Ǧ������Ϊb����ԭҺ����Ǧ�������ʵ���Ϊc/2bmol������Ǧ�����ʵ���ҲΪc/2bmol������Ϊ239c/2bg��Ǧ���������Ϊag������������Ϊ
PbCl42-(aq)����ˮϡ�ͣ�������Ũ�Ƚ��ͣ�ƽ�������ƶ�����ȴ���¶Ƚ��ͣ� PbCl2�ܽ�ȼ�С���Ӷ�����PbCl2���塣(5) ����Һ3�Ǻ���PbCl42-����Һ��Ҫ�Ƶõ���Ǧ��Ԫ��Ǧ�Ļ��ϼ۽��ͣ��õ����ӣ�������ԭ��Ӧ�����ݵ��صĹ���ԭ���������õ����ӣ�����Һ3Ӧ���������ҡ�������������Һ2����Һ2���Ȼ�������Һ����������������ʧȥ���ӣ�ת��Ϊ�����ӣ��缫��Ӧ��Fe2+- e-= Fe3+��ʹc(Fe3+)���ߣ���Һ�е�������������ͨ�������ӽ���Ĥ���ﵽ�����ң��������ӽ�ϣ��õ��Ȼ���������Pb2+--Pb��1mol Pb2+ת��2mol���ӣ���������ͨ��cmol����ʱ������Ǧȫ�����������Ծ���c/2mol��Ǧ������Ǧ������Ϊb����ԭҺ����Ǧ�������ʵ���Ϊc/2bmol������Ǧ�����ʵ���ҲΪc/2bmol������Ϊ239c/2bg��Ǧ���������Ϊag������������Ϊ![]() ��
��

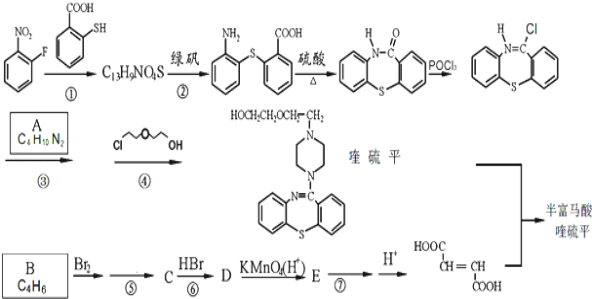
����Ŀ�������ܿ�����ָʾ���ʹ������Ʊ�����ˮ�ܿ���Ҫ�ɷ�ΪCo2O3��������Fe2O3��A12O3��MnO��MgO��CaO��SiO2�ȣ���ȡCoC2O4��2H2O�����������£�
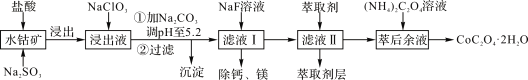
��֪���ٽ���Һ���е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Ca2+��Mg2+��Al3+�ȣ�
�����������£�ClO3-��������Co2+��ClO3-ת��ΪCl-��
�۲���������������������ʽ����ʱ��Һ��pH������
������ | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
��ȫ������pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
��1�����������м���Na2SO3����ҪĿ����________��
��2�������Һ�м���NaClO3�����ӷ�Ӧ����ʽ��_________��
��3����֪��������NH3��H2O![]() NH4+��OH- Kb��1.8��10-5
NH4+��OH- Kb��1.8��10-5
H2C2O4![]() H+��HC2O4- Ka1��5.4��10-2
H+��HC2O4- Ka1��5.4��10-2
HC2O4-![]() H��C2O42- Ka2��5.4��10-5
H��C2O42- Ka2��5.4��10-5
�������������(NH4)2C2O4��Һ��pH______7�������������=������
��4������(NH4)2C2O4 ��Һ���������壬�ٹ��ˡ�ϴ�ӣ�ϴ��ʱ��ѡ�õ��Լ��У�________��
A������ˮ B������ˮ C�����͵�(NH4)2C2O4��Һ D��ϡ����
��5����ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ����ͼ1����ȡ����������________����ʹ�õ�����pH��Χ��________��
A��2.0��2.5 B��3.0��3.5 C��4.0��4.5
��6��CoC2O4��2H2O�ȷֽ������仯������ͼ2��ʾ������600����ǰ�Ǹ����������ȣ�600 ���Ժ����ڿ����м��ȡ�A��B��C��Ϊ�����C����ʾ����Ļ�ѧʽ��________��