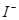题目内容
已知在室温时,Mg(OH)2的溶度积Ksp=5.6×10-12 (mol/L)3,要使0.2mol/lMgSO4溶液中的Mg2+沉淀较为完全[c(Mg2+)<5.6×10-6mol/L],则应向溶液中加入NaOH溶液,使溶液的pH最小为多少?
11
试题分析:当溶液中c(Mg2+)<5.6×10-6mol/L时可以视为完全沉淀
则根据氢氧化镁的溶度积常数表达式Ksp=c(Mg2+)·c2(OH-)可知
此时c(OH-)=
 =
=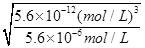 =1.0×10-3mol/L
=1.0×10-3mol/L所以溶液中氢离子浓度是1.0×10-3mol/L
由此溶液的pH=11

练习册系列答案
相关题目



 mMn+(aq) + nAm-(aq),Ksp=[c(Mn+)]m·[c(Am-)]n。
mMn+(aq) + nAm-(aq),Ksp=[c(Mn+)]m·[c(Am-)]n。
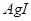 沉淀中滴入浓KCI溶液有白色沉淀出现
沉淀中滴入浓KCI溶液有白色沉淀出现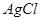 比
比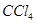 振荡,静置,下层溶液为紫色
振荡,静置,下层溶液为紫色