题目内容
4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在10L密闭容器中进行,10s后,水蒸气的物质的量增加了0.60mol,则此反应的平均速率
(X)(反应物的消耗速率或产物的生成速率)可表示为( )
- v |
A、
| ||
B、
| ||
C、
| ||
D、
|
分析:根据v=
计算v(H2O),再利用速率之比等于化学计量数之比计算各物质表示的反应速率,进行判断.
| ||
| △t |
解答:解:在体积10L的密闭容器中进行,10s后,水蒸气的物质的量增加了0.6mol,
则v(H2O)=
=0.006mol/(L?s),
A.速率之比等于化学计量数之比,所以v(NH3)=
×0.006mol/(L?s)=0.004mol/(L?s),故A错误;
B.速率之比等于化学计量数之比,所以v(NO)=
×0.006mol/(L?s)=0.004mol/(L?s),故B正确;
C.速率之比等于化学计量数之比,所以v(O2)=
×0.006mol/(L?s)=0.005mol/(L?s),故C错误;
D.v(H2O)=0.006mol/(L?s)=0.36mol/(L?min),故D错误.
故选:B.
则v(H2O)=
| ||
| 10s |
A.速率之比等于化学计量数之比,所以v(NH3)=
| 2 |
| 3 |
B.速率之比等于化学计量数之比,所以v(NO)=
| 2 |
| 3 |
C.速率之比等于化学计量数之比,所以v(O2)=
| 5 |
| 6 |
D.v(H2O)=0.006mol/(L?s)=0.36mol/(L?min),故D错误.
故选:B.
点评:本题考查化学反应速率的计算,难度不大,注意公式的运用,化学反应速率的计算通常有定义法、化学计量数法,根据题目选择合适的计算方法.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(X)(反应物的消耗速率或生成物的生成速率)可表示为( )
| A、v(NH3)=0.010 mol?(L?s)-1 | B、v(O2)=0.001 mol?(L?s)-1 | C、v(NO)=0.0010 mol?(L?s)-1 | D、v(H2O)=0.045 mol?(L?s)-1 |
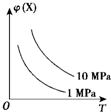 如图所示,φ(X)为气态反应物在平衡混合物中的体积分数,T为温度.符合该曲线的反应是( )
如图所示,φ(X)为气态反应物在平衡混合物中的体积分数,T为温度.符合该曲线的反应是( )| A、N2(g)+3H2(g)?2NH3(g)△H<0 | B、H2(g)+I2(g)?2HI(g)△H<0 | C、4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 | D、C(s)+H2O(g)?H2(g)+CO(g)△H>0 |

 、
、 、
、 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是