题目内容
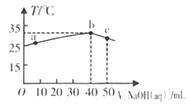
【题目】25℃时,将0.1mo/L的NaOH溶液滴入盛有50mL pH= 2的H A溶液的绝热容器中,加入NaOH溶液的体积V与溶液温度T的关系如下图。下列说法正确的是
A. a点溶液中,c(A-)+ c(HA)= 0.08mol/L.
B. b点溶液中,c(A-)<c(Na+))
C. b → c的过程中,发生了吸热反应
D. 溶液中HA的电离平衡常数a点等于b点
【答案】B
【解析】酸碱中和放热,b点温度最高,所以b点是NaOH与HA恰好反应的点;40mL0.1mo/L的NaOH溶液与50mL pH= 2的H A溶液恰好反应,所以HA的浓度是![]() 0.08mo/L。根据物料守恒,a点溶液中c( A-)+ c(HA)=
0.08mo/L。根据物料守恒,a点溶液中c( A-)+ c(HA)= ![]() 0.067 mol/L ,故A错误;0.08mo/L的HA溶液pH= 2,说明HA是弱酸,NaA是强碱弱酸盐,所以b点溶液中c( A-)<c(Na+),故B正确;b
0.067 mol/L ,故A错误;0.08mo/L的HA溶液pH= 2,说明HA是弱酸,NaA是强碱弱酸盐,所以b点溶液中c( A-)<c(Na+),故B正确;b![]() c的过程没有发生反应,温度降低的原因是35℃的NaA溶液中又加入10mL 25℃的NaOH溶液,故C错误;b点温度大于a点,所以HA的电离平衡常数a点小于b点,故D错误。
c的过程没有发生反应,温度降低的原因是35℃的NaA溶液中又加入10mL 25℃的NaOH溶液,故C错误;b点温度大于a点,所以HA的电离平衡常数a点小于b点,故D错误。

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】用0.001mol/L的酸性高锰酸钾溶液滴定未知浓度的草酸(H2C2O4)溶液,回答下列 问题:
(1)酸性高锰酸钾溶液应该装在下图__________滴定管中。

(2)请写出该反应的离子方程式:____________________。
(3)用0.001mol/L的酸性高锰酸钾溶液滴定草酸溶液,滴定终点的判断依据是:_________________。
(4)己知滴定V1ml待测液消耗标准液实验数据如下表
实验次数 | 始读数(ml) | 末读数(ml) | 消耗体积 |
1 | 0.10 | 19.20 | 19.10 |
2 | 1.85 | 20.75 | 18.90 |
3 | 0.00 | 24.06 | 24.06 |
则待测液的浓度为:_______________
(5)滴定结束时,俯视刻度线读取高锰酸钾溶液的体积,会导致测定结果_________(填“偏大”“偏小”或“不影响”)
(6)己知NaHC2O4溶液中草酸氢根离子的电离大于水解,则溶液中各离子的浓度按由大到小的顺序排列的是:_________________________。