��Ŀ����
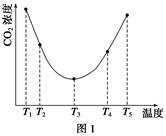
ij�¶�ʱ��2L������X��Y��Z������̬���ʵ����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ�����
��1���÷�Ӧ�Ļ�ѧ����ʽΪ��
��2����Ӧ��ʼ��2min����X��ʾ��ƽ����Ӧ����Ϊ��
��3������������˵��������Ӧ�ﵽ��ѧƽ��״̬���� ������ĸ��
A���������������ʵ�������ʱ��ı仯���仯
B����λʱ����ÿ����3mol X��ͬʱ����2mol Z
C��������������������ʱ��ı仯���仯
��4�����ܱ������ͨ��a mol X(g)��b mol Y(g)��������ӦX(g��+ Y(g��=2Z(g)�����ı���������ʱ����Ӧ���ʻᷢ��ʲô�仯��ѡ������� ��С�� ���䡱��
�� �����¶ȣ�
�ڱ���������������䣬����X(g)�����ʵ�����
�� ���������������
��1��3X+Y 2Z(��д������Ų�����)
2Z(��д������Ų�����)
��2��0.075mol?L-1?min-1
��3��A
��4���ټ�С������ۼ�С
���������������1����ͼ��֪��X��Y�Ƿ�Ӧ����ʵ����ֱ����0.3mol��0.1mol��Z����������ʵ�������0.2mol����ʽ��X��Y��Z�����ʵ�������3:1:2�����Ը÷�Ӧ�Ļ�ѧ����ʽΪ��3X+Y 2Z
2Z
��2��X��Ũ�ȼ���0.3mol/2L="0.15mol/L," ���Է�Ӧ��ʼ��2min����X��ʾ��ƽ����Ӧ����Ϊ0.15mol/L/2min=0.075mol?L-1?min-1
(3)A���÷�Ӧ����������ʵ�����С�ķ�Ӧ�����ﵽ��ѧƽ��ʱ���������������ʵ�������ʱ��ı仯���仯����ȷ��B����Ӧ���κ�ʱ�̶��е�λʱ����ÿ����3mol X��ͬʱ����2mol Z�������ж��Ƿ�ﻯѧƽ��״̬������C���κλ�ѧ��Ӧ����ѭ�����غ㶨�ɣ�����ѡA��
��4�����������Է�Ӧ���ʵ�Ӱ�죬�ٽ����¶ȣ���Ӧ���ʼ�С��������Ӧ���Ũ�ȣ���Ӧ����������������������൱�ڼ�Сѹǿ����Ӧ���ʼ�С��
���㣺���黯ѧ����ʽ���Ƶ�����Ӧ���ʵļ��㣬��ѧƽ��״̬���жϣ������Է�Ӧ���ʵ�Ӱ��

ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�
��1����ˮ����ͨ�����ȵ�̿���ɲ���ˮú������ӦΪ��C(s)��H2O(g)  CO(g)��H2(g) ��H����131.3 kJ��mol��1һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���� (����ĸ����ͬ)
CO(g)��H2(g) ��H����131.3 kJ��mol��1һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���� (����ĸ����ͬ)
A�������е�ѹǿ����
B��1 mol H��H�����ѵ�ͬʱ����2 mol H��O��
C��v��(CO)��v��(H2O)
D��c(CO)��c(H2)
��2������ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2 L�ĺ����ܱ������У����з�ӦCO(g)��H2O(g)  CO2(g)��H2(g)���õ������������ݣ�
CO2(g)��H2(g)���õ������������ݣ�
| ʵ �� �� | �� �� /�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�ٸ÷�Ӧ���淴ӦΪ (������š�)�ȷ�Ӧ��
����ʵ��3Ҫ�ﵽ��ʵ��2��ͬ��ƽ��״̬(�������ʵ����������ֱ����)����t<3 min����a��bӦ����Ĺ�ϵ�� (�ú�a��b����ѧʽ��ʾ)��
(3)Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��CO2(g)+3H2(g)
 CH3OH(g) +H2O(g)����ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ��mol��1)�ı仯�������Ϊ1 L�ĺ����ܱ������У�����1 mol CO2��3 mol H2�� ���д�ʩ����ʹ c(CH3OH)�������
CH3OH(g) +H2O(g)����ͼ��ʾ�÷�Ӧ���й���������(��λΪkJ��mol��1)�ı仯�������Ϊ1 L�ĺ����ܱ������У�����1 mol CO2��3 mol H2�� ���д�ʩ����ʹ c(CH3OH)������� 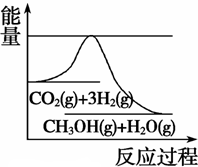
A�������¶�
B������N2(g)��ʹ��ϵѹǿ����
C����H2O(g)����ϵ�з������
D���ٳ���0.5 mol CO2��1.5 mol H2
����ͼ��ʾװ�ý�������ʵ��:
(1)�ڼ��װ�õ������Ժ�,���Թ�a�м���10 mL 6 mol��L-1��ϡ�����1 gͭƬ,�����ô��е��ܵ���Ƥ�������Թܿڡ���д�����Թ�a���п��ܷ��������з�Ӧ�Ļ�ѧ����ʽ����
(2)��ʵ������г�����Ӧ��ʼʱ���ʻ���,����ӿ�,����������������������������,����Ӧ����һ��ʱ�������������,ԭ��������
(3)���Ͽ���Ƶ�NO,�ɲ�ȡ�Ĵ�ʩ��������(��д��ĸ���)��
| A������ | B��ʹ��ͭ�� | C��ϡ��HNO3 | D�����������Ũ�� |
�¶�ΪTʱ����2.0 L�����ܱ������г���1.0 mol PCl5����ӦPCl5(g)��PCl3(g)��Cl2(g)����һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
����˵����ȷ���� (����)
A����Ӧ��ǰ50 s ��ƽ������v(PCl3)�� 0.0032 mol��L��1��s��1
B�����������������䣬�����¶ȣ�ƽ��ʱc(PCl3)�� 0.11 mol��L��1����Ӧ�Ħ�H<0
C����ͬ�¶��£���ʼʱ�������г���1.0 mol PCl5��0.20 mol PCl3��0.20 mol Cl2����Ӧ�ﵽƽ��ǰv(��)>v(��)
D����ͬ�¶��£���ʼʱ�������г���2.0 mol PCl3��2.0 mol Cl2���ﵽƽ��ʱ��PCl3��ת���ʴ���80%
 xC(g)��2 minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ����0.8 mol B�������C��Ũ��Ϊ0.4 mol��L��1������д���пհף�
xC(g)��2 minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ����0.8 mol B�������C��Ũ��Ϊ0.4 mol��L��1������д���пհף� pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C����������Ҳ��С����:
pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C����������Ҳ��С����: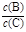 �� ��
�� �� H2����I2
H2����I2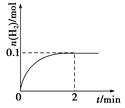
 3B(��)��C(��)�������仯��ͼ����ʾ�������ƽ����Է���������ʱ��ı仯��ͼ����ʾ��
3B(��)��C(��)�������仯��ͼ����ʾ�������ƽ����Է���������ʱ��ı仯��ͼ����ʾ��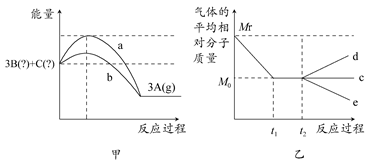
 (NH4)2CO3(aq)��H1
(NH4)2CO3(aq)��H1